
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1100 | 841 | 680 | 533 | 409 |
分析 在水溶液中橙色的Cr2O72-与黄色的CrO42-存在如下平衡:Cr2O72-+H2O?2CrO42-+2H+,当改变一个条件,平衡会向减弱这种改变的方向进行,
(1)向甲试管中加入NaOH溶液,中和氢离子,氢离子浓度降低,平衡正向移动;
(2)向乙试管中加入足量Ba(NO3)2溶液,溶液中钡离子结合CrO42-形成BaCrO4为黄色沉淀,平衡正向进行;
解答 解:(1)向甲试管中加入NaOH溶液,中和平衡状态下的氢离子,氢离子浓度降低,平衡正向移动,所以上述平衡向方向正反应,
故答案为:正反应;
(2)向乙试管中加入足量Ba(NO3)2溶液,溶液中钡离子不断结合CrO42-形成BaCrO4为黄色沉淀,促使平衡正向进行彻底,最后溶液显无色,
故答案为:无;
点评 本题考查化学平衡的影响因素,比较基础,注意对化学平衡移动原理的理解和应用,熟练掌握基础知识是解题关键.


科目:高中化学 来源:2016-2017学年湖南省高二上第三次月考化学卷(解析版) 题型:选择题
反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在2L的密闭容器中进行,1min后,NH3减少了0.12mol,则平均每秒钟浓度变化正确的是
A.NO:0.06mol•L﹣1  B.H2O:0.002mol•L﹣1
B.H2O:0.002mol•L﹣1
C.NH3:0.002mol•L﹣1 D.O2:0.00125mol•L﹣1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上第一次月考化学卷(解析版) 题型:选择题
已知反应①:CO(g)+CuO(s) CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②:H2(g)+CuO(s) Cu(s)+H2O(g)在相同的温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是
CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是
A.反应①的平衡常数K1=[c(C O2)•c(Cu)]/[c(CO)•c(CuO)]
O2)•c(Cu)]/[c(CO)•c(CuO)]
B.对于反应③,恒容时,温度升高,H2的浓度减小,则该反应的焓变为正值
C.反应③的平衡常数K=K1/K2
D.对于反应③,恒温恒容下,增大压强,H2的浓度一定减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上第一次月考化学卷(解析版) 题型:选择题
在密闭容器中充入一定量的N02,发生反应2N02(g) N204(g) △H=一57kJ·mol—1。在温度为T1、T2时,平衡体系中N02的体积分数随压强变化的曲线如图所示。下列说法正确的是 ( )
N204(g) △H=一57kJ·mol—1。在温度为T1、T2时,平衡体系中N02的体积分数随压强变化的曲线如图所示。下列说法正确的是 ( )
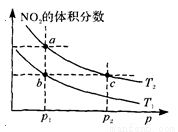
A.a、c两点的反应速率:a>c
B.a、b两点N02的转化率:a<b
C.a、c两点气体的颜色:a深,c浅
D.由a点到b点,可以用加热的方法
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 气体1可能为NO和CO2的混合物 | |
| B. | 沉淀3可能为Mg(OH)2和Al(OH)3的混合物 | |
| C. | 沉淀4可能为BaCO3、BaSO3或二者混合物 | |
| D. | X中一定有K2SO3,可能有KAlO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极发生的电极反应为:3O2+6CO2+12e-═6CO${\;}_{3}^{2-}$ | |
| B. | 通入乙烯的一极为正极 | |
| C. | 负极发生的电极反应为:CH2=CH2+6CO${\;}_{3}^{2-}$-12e-═8CO2+2H2O | |
| D. | 电池的总反应式为:CH2=CH2+3O2═2CO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大多数化学反应在一定条件下都有一定的限度 | |
| B. | 当可逆反应达到反应限度时,反应会自动停止 | |
| C. | 使用催化剂,可降低反应的活化能,加快反应速率,改变反应限度 | |
| D. | FeCl3与KSCN反应达到平衡时,向其中加少量KCl固体,则溶液颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀H2SO4 | B. | 稀HNO3 | C. | 浓H2SO4 | D. | 稀HCl(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com