
【题目】某恒定温度下,在一个2L的密闭容器中充入A气体、B气体,其浓度分别为2 mol/L,1 mol/L,且发生如下反应:3A(g)+2B(g) 4C(?)+2D(?)已知“?”代表C、D状态未确定;反应一段时间后达到平衡,测得生成1.6 mol C,且反应前后压强比为5:4,则下列说法中正确的是( )
①该反应的化学平衡常数表达式为:![]()
②此时B的转化率为35%
③增大该体系压强,平衡向右移动,但化学平衡常数不变
④增加C的量,A、B转化率不变
A. ①②B. ②③C. ③④D. ①④
【答案】C
【解析】
反应一段时间后达到平衡,测得反应前后压强比为5:4,故反应后气体体积减小,故C、D至少一种不为气体;在一个2L的密闭容器中充入A气体,B气体,测得其浓度为2mol/L和1mol/L;则A气体,B气体的物质的量分别为2mol/L×2L=4mol,1mol/L×2L=2mol,则反应前气体总的物质的量为4mol+2mol=6mol;测得反应前后压强比为5:4,故平衡时气体总的物质的量为6mol×4/5=4.8mol;生成1.6molC,则生成D的物质的量为1.6×2/4=0.8mol,反应的B的物质的量为1.6×2/4=0.8mol,反应A的物质的量为1.6×3/4=1.2mol,则平衡时,A、B、C、D的物质的量分别为4mol-1.2mol=2.8mol、2mol-0.8mol=1.2mol、1.6mol、0.8mol,平衡时气体总的物质的量为6mol×![]() =4.8mol,故D为气体,C不为气体.①C不为气体,故C不能出现在平衡常数的表达式中,故①错误;②反应的B的物质的量为0.8mol,故B的平衡转化率为
=4.8mol,故D为气体,C不为气体.①C不为气体,故C不能出现在平衡常数的表达式中,故①错误;②反应的B的物质的量为0.8mol,故B的平衡转化率为![]() ×100%=40%,故②错误;③反应后气体体积减小,故增大该体系压强,平衡向右移动;平衡常数与温度有关,温度不变,化学平衡常数不变,故③正确;④C不为气体,故增加C的量,平衡不移动,故A、B转化率不变,故④正确;故说法中正确的是③④,答案选C。
×100%=40%,故②错误;③反应后气体体积减小,故增大该体系压强,平衡向右移动;平衡常数与温度有关,温度不变,化学平衡常数不变,故③正确;④C不为气体,故增加C的量,平衡不移动,故A、B转化率不变,故④正确;故说法中正确的是③④,答案选C。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D的原子序数依次增大。甲、乙、丙、丁、戊是这四种元素组成的常见化合物,己是元素C 的单质。已知甲、乙的焰色均为黄色且水溶液均呈碱性,它们之间的转化关系如图所示。下列说法不正确的是

A. 甲和乙加入水中都能促进水的电离平衡
B. 乙和戊都是离子化合物
C. 离子半径:C>D>A
D. A、B、C形成化合物的水溶液一定呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.液氨用作制冷剂发生的是化学反应
B.氨气溶水得到氨水发生的只是物理变化
C.分离液态空气制取氮气属于氮的固定
D.氮气与氢气化合生成氨气属于人工固氮
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产需要大量原料,消耗大量能源,在得到所需产品同时产生了大量废气、废水、废渣。某工厂排放的废水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,准备回收废水中的铜和汞,同时得到绿矾。他们设计了如下实验方案:
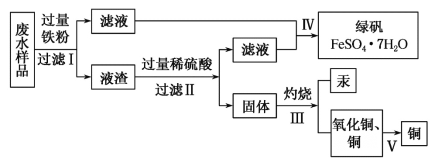
(1)现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的玻璃仪器是__________设计简单实验检验绿矾是否变质,简述你的操作:__________。
(2)步骤Ⅰ中加入过量铁粉的目的是__________,步骤Ⅱ中__________(填“能”或“不能”)用盐酸代替硫酸。
(3)步骤V利用氧化铜制取铜有如下四种方案:
方案甲:利用氢气还原氧化铜;
方案乙:利用一氧化碳还原氧化铜;
方案丙:利用炭粉还原氧化铜;
方案丁:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。
从安全角度考虑,方案__________不好;从产品纯度考虑,方案__________不好。
(4)写出步骤Ⅱ中涉及反应的离子方程式:__________;步骤Ⅳ得到绿矾的操作蒸发浓缩__________、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、体积为2L的密闭容器中加入1molCO2和3molH2,发生如下的反应:CO2(g) +3H2(g)![]() CH3OH(g) +H2O(g) △H<0。可认定该可逆反应在一定条件下已达到化学平衡状态的是( )
CH3OH(g) +H2O(g) △H<0。可认定该可逆反应在一定条件下已达到化学平衡状态的是( )
A. 容器中CO2、H2、CH3OH、H2O的物质的量之比为1∶3∶1 ∶1B. v正(CO2)=v逆(H2O)
C. 容器内混合气体密度保持不变D. 3molH-H键断裂同时断裂3molH-O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上冶炼钛的有关反应如下所示:
① C(s) + O2(g) ![]() CO2(g) ΔH1
CO2(g) ΔH1
② 2CO(g) + O2(g) ![]() 2CO2(g) ΔH2
2CO2(g) ΔH2
③ TiO2(s) + 2Cl2(g) ![]() TiCl4(g) + O2(g) ΔH3
TiCl4(g) + O2(g) ΔH3
④ TiCl4(s) + 2Mg(s) ![]() 2MgCl2(s) + Ti(s) ΔH4
2MgCl2(s) + Ti(s) ΔH4
⑤ TiO2(s) + 2Cl2(g) + 2C(s) ![]() TiCl4(g) + 2CO(g) ΔH5
TiCl4(g) + 2CO(g) ΔH5
下列有关推断正确的是( )
A. 2ΔH1=ΔH2 B. ΔH1<0,ΔH2>0
C. ΔH5=ΔH3+2ΔH1-ΔH2 D. 2ΔH1-ΔH2>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积固定的VL密闭容器中充入4molNH3和5molO2,发生如下反应:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g)。请回答下列问题:
4NO(g)+6H2O(g)。请回答下列问题:
(1)下列能说明该反应已经达到平衡状态的是_______;
A 容器中气体总质量不变
B c(O2)不变
C v(O2)=1.25v(NH3)
D 体系压强不变
E 相同时间内,消耗0.1 mol NH3,同时消耗了0.1 mol NO
(2)若反应在绝热密闭系统中进行时,其余条件不变,反应速率是先增大后减小。则速率逐渐增大是因为______,速率又逐渐减小的原因是_____。
(3)1mol NH3(g)在纯氧中完全燃烧生成无污染的气态物质,放出akJ的热量。写出该反应的热化学方程式__________________________________________。
(4)若将(3)所述反应设计为电解质溶液为KOH的原电池,则负极反应式 _________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.离子化合物中可能含有共价键
B.分子晶体中的分子内不含有共价键
C.分子晶体中一定有非极性共价键
D.分子晶体中分子一定紧密堆积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com