

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
| W | |||||||
| X | Y | Z |



查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
 Al(OH)3+OH-
Al(OH)3+OH- Al(OH)3+OH-
Al(OH)3+OH-查看答案和解析>>
科目:高中化学 来源: 题型:
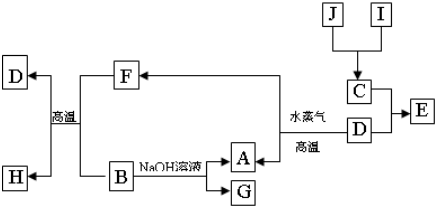
 (2012?河西区二模)A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.A元素的原子半径最小,与E同主族,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐X,D与E可形成淡黄色固体Y,F元素原子的最外层电子数比次外层电子数少1.请按要求回答下列问题:
(2012?河西区二模)A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大.A元素的原子半径最小,与E同主族,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物对应的水化物与其氢化物反应能生成盐X,D与E可形成淡黄色固体Y,F元素原子的最外层电子数比次外层电子数少1.请按要求回答下列问题:

查看答案和解析>>
科目:高中化学 来源:江西省重点中学协作体2010届高三第二次联考(化学) 题型:填空题
短周期元素W、X、Y、Z、在元素周期表中的位置如图所示,
| W | | | | | | | |
| | | | X | Y | Z | | |
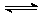 Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间
Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间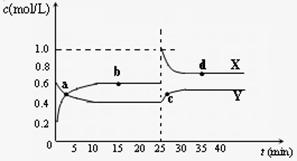 的变化关系如右图所示。
的变化关系如右图所示。查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素W、X、Y、Z、在元素周期表中的位置如图所示,
| W | |||||||
| X | Y | Z |
其中X、Y、Z三种元素的质子数之和为21。?
(1)W与Z形成原子个数比为1∶1的化合物,其电子式为 。
(2)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈
酸性,其原因是 (用化学用语表示);
该溶液中各种离子浓度由大到小的顺序为 。
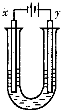
(3)由X W4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为
。
(4)已知:2YZ2(g) ![]() Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间
Y2Z4(g);△H<0。在恒温恒容条件下,将一定量XZ2和X2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间
t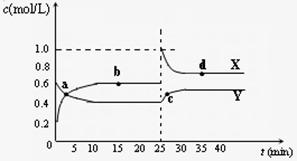 的变化关系如右图所示。
的变化关系如右图所示。
① a、b、c、d四个点中,化学反应
处于平衡状态的是 点。
② 25 min时,增加了
(填物质的化学式) mol。
③ a、b、c、d四个点中所表示的反应体系
中,气体颜色由深到浅的顺序是 __
(填字母)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com