
| A. | 1:9 | B. | 1:49 | C. | 1:99 | D. | 以上都不正确 |
分析 氢氧化钡和硫酸氢钠反应钡离子恰好沉淀,需要Ba(OH)2和NaHSO4按照物质的量1:1反应,结合溶液的pH和溶液体积换算物质的量列式计算.
解答 解:pH=13的Ba(OH)2溶液中C(OH-)=10-1mol/L,设溶液体积为x,则含有的氢氧根离子物质的量为0.1xmol,含有的Ba2+的物质的量为0.05xmol,由于逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀,故反应的硫酸氢钠物质的量为:0.05xmol.
设硫酸氢钠溶液体积为y,依据反应Ba(OH)2+NaHSO4=BaSO4↓+H2O+NaOH,混合后溶液pH=11,则反应后溶液中氢氧根离子浓度为10-3mol/L,
即:$\frac{0.1x-0.05x}{x+y}$=10-3,
整理可得:x:y=1:49,
故所加入的Ba(OH)2溶液与NaHSO4溶液体积之比是1:49.
故选B.
点评 本题考查了酸碱反应的综合计算、溶液pH的计算应用,题目难度中等,明确溶液中氢氧根离子浓度和溶质浓度的关系是解题关键,注意掌握溶液酸碱性与溶液pH的计算方法.


科目:高中化学 来源: 题型:多选题
| A. | 丙烯分子中有8个σ键,1个π键 | |
| B. | 在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 | |
| C. | NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力 | |
| D. | NCl3和BC13分子中,中心原子都采用sp3杂化 | |
| E. | 在“冰→水→水蒸气→氧气和氢气”的变化过程中,各阶段被破坏的粒子间主要的相互作用依次是氢键、分子间作用力、极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.4mol | B. | 0.3 mol | C. | 0.2mol | D. | 0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
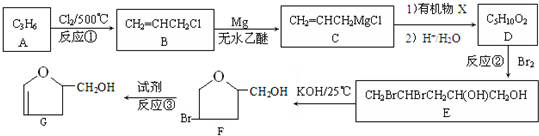
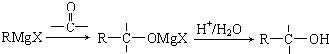
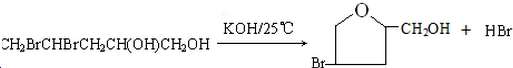 (或
(或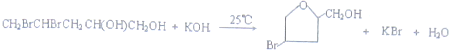 );;
);;查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 化学式 | 颜色 | Ksp |
| AgCl | 白色 | 2.0×10-10 |
| AgBr | 浅黄色 | 5.4×10-13 |
| AgI | 黄色 | 8.3×10-17 |
| Ag2S | 黑色 | 2.0×10-48 |
| Ag2CrO4 | 红色 | 2.0×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
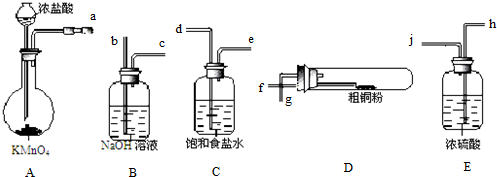

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com