
短周期元素甲和乙,甲原子的最外层电子数为a,次外层电子数为b;乙原子的M层电子数为(a–b),L层电子数为(a+b)。则甲、乙两元素形成的化合物具有的性质是( )
A.与水反应 B.与氢氧化钠溶液反应
C.与硫酸反应 D.与前三种物质均能反应
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源:2015-2016学年福建省高二上学期期中测试化学试卷(解析版) 题型:填空题
某化学反应2A(g) B(g)+D(g)在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如表:
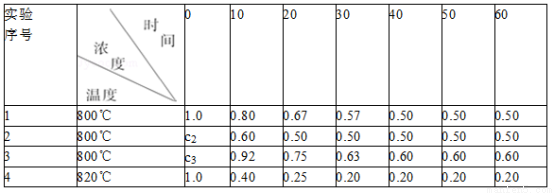
根据上述数据,完成下列填空:
(1)实验1,反应在10至20分钟时间内A平均速率为______________ .
(2)实验2,A的初始浓度c2=____________mol·L-1,推测实验2中还隐含的条件是____________
(3) 800 ℃时该反应的平衡常数K=___________________
(4)设实验3的反应速率为v3,实验1的反应速率为v1,则v3___________v1(填>、<、=),且C3=_________mol·L-1.
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市高三上学期10月阶段测化学试卷(解析版) 题型:选择题
下列物质的转化在给定条件下能实现的是
①Al2O3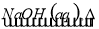 NaAlO2(aq)
NaAlO2(aq)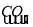 Al(OH)3
Al(OH)3
②SO2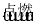 SO3
SO3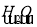 H2SO4
H2SO4
③Fe2O3 FeCl3(aq)
FeCl3(aq) 无水FeCl3
无水FeCl3
④饱和NaCl(aq)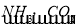 NaHCO3
NaHCO3  Na2CO3
Na2CO3
⑤MgCl2(aq)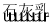 Mg(OH)2
Mg(OH)2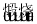 MgO
MgO
A、①③⑤ B、②③④ C、②④⑤ D、①④⑤
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第四次考试化学试卷(解析版) 题型:选择题
元素X~Z是元素周期表中4种主族元素,其性质或结构信息如下表,有关下列元素的描述错误的是
元素 | X | Y | W | Z |
相关信息 | 用硫酸处理海藻灰时,可得通常状况下为紫黑色的固体,其制剂可用来消毒 | 工业上在冰晶石存在的条件下,用电解法制取其单质 | 最早是在用氯气处理提取食盐后的盐水母液中发现的,被称作“海洋元素” | 原子的电子总数是最外层电子数的6倍 |
A.实验室可在海藻灰的浸出液中滴加双氧水来制取元素X的单质
B.元素X、Y的单质充分混合后滴加少量水,可看到大量紫色蒸汽生成,说明该反应会放出大量的热
C.元素X的气态氢化物的沸点高于元素W的气态氢化物的沸点
D.元素Z是一种较活泼的金属元素,可用铝热法从Z的氧化物中制备Z的单质
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第三次考试化学试卷(解析版) 题型:选择题
如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是

A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色
B.若A为浓氨水,B为生石灰,C中盛A1C13溶液,则C中先产生白色沉淀后沉淀又溶解
C.若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
D.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊试液,则C中溶液先变红后褪色
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三第四次(12月)月考化学试卷(解析版) 题型:填空题
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。
(1)Fe基态核外电子排布式为 。
(2)科学研究表明用TiO2作光催化剂可将废水中CN-转化为OCN-、并最终氧化为N2、CO2。OCN-中三种元素的第一电离能由大到小的顺序为 。
(3)与OCN-互为等电子体的一种分子为 (填化学式)
(4)铁元素还能与一些氨基酸形成配合物,羧基中碳原子的杂化类型是 ;1mol乙酸中含有σ键的数目为 。
(5)铁铝合金的一种晶体属于面心立方结构,其晶胞可看成由8个小体心立方结构堆砌而成。已知小立方体如图所示。该合金的化学式为 。
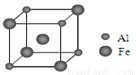
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷(解析版) 题型:填空题
(1)写出下列物质的化学式:硫铁矿 石膏
(2)SiO2是硅最重要的化合物,其用途是 (举一例)
(3)已知1g乙醇完全燃烧生成液态水放出29.7kJ的热量,写出乙醇燃烧热的热化学方程式 。
(4)配平化学方程式:___K2Cr2O7+___HCl——___KCl+___CrCl3+___Cl2↑+___H2O
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中考试化学试卷(解析版) 题型:填空题
七铝十二钙(12CaO•7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:

(1)煅粉主要含MgO和 ;用适量的NH4NO3溶液浸取煅粉后,镁化合物几乎不溶,该工艺中不能用(NH4)2SO4代替NH4NO3,原因是 。
(2)滤液I中的阴离子有 (忽略杂质成分的影响);若滤液I中仅通入CO2,会生成 ,从而导致CaCO3产率降低。
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为 。
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高二上期中考试化学试卷卷(解析版) 题型:选择题
向某密闭容器中加入0.3 mol A、0.1 mo l C和一定量的B三种气体。一定条件下发生反应,各物质的浓度随时间变化如甲图所示[t0~t1阶段的c(B)变化未画出]。乙图
l C和一定量的B三种气体。一定条件下发生反应,各物质的浓度随时间变化如甲图所示[t0~t1阶段的c(B)变化未画出]。乙图 为t2时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,t3时刻为使用催化剂。下列说法中正确的是
为t2时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,t3时刻为使用催化剂。下列说法中正确的是
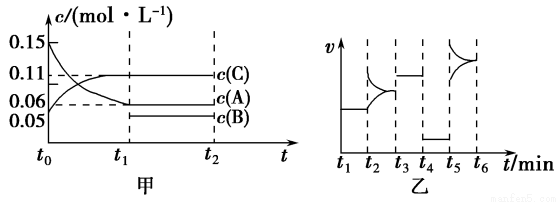
A.若t1=15 s,用A的浓度变化表示t0~t1阶段的平均反应速率为0.004 mol·L-1·s-1
B.t4~t5阶段改变的条件一定为减小压强
C.该容器的容积为2 L,B的起始物质的量为0.02 mol
D.t5~t6阶段,若容器内A的物质的量减少了0.06 mol,而此过程中容器与外界的热交换总量为a kJ,该反应的热化学方程式3A(g) B(g)+2C(g)ΔH=-50a kJ·mol-1
B(g)+2C(g)ΔH=-50a kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com