
有机化工原料1,4-二苯基-1,3-丁二烯及某抗结肠炎药物有效成分的合成路线如(部分反应略去试剂和条件):已知:


(1)抗结肠炎药物有效成分分子中的含氧官能团名称是__________。
(2)D 的结构简式是_______________。
(3)写出F 与NaOH 反应的化学方程式_____________。
(4)下列说法正确的是________(填选项字母)。
A.④的反应条件X 和⑤的反应条件Y 完全相同
B.①②④⑤反应类型相同
C.G 不可以发生缩聚反应
D .设计D→E 和F→G 两步反应的目的是防止酚羟基被氧化
.设计D→E 和F→G 两步反应的目的是防止酚羟基被氧化
(5)③的化学方程式是___________。
(6)E 有多种同分异构体,符合下列条件的同分异构体有___________种 。
①结构中有苯环 ②与E 有相同的官能团 ③不能发生银镜反应
(7)1,4-二苯基-1,3-丁二烯有多种同分异构体,写出符合下列条件的同分异构体的结构简式:
a.结构中有两个苯环,无其它环状结构。
b.苯环上的一硝基取代产物有两种。
c.其核磁共振氢谱有3 种峰,峰面积之比为3∶2∶2。
科目:高中化学 来源:2015-2016学年辽宁庄河高中高二下期末化学试卷(解析版) 题型:选择题
某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42﹣、NO3﹣、Cl﹣中的4种离子,所含离子的物质的量均为1mol.若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法不正确的是( )
A.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g
B.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色
C.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色
D.该溶液中所含的离子是:Fe2+、Na+、SO42﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省松原市高二下期末化学试卷(解析版) 题型:实验题
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:
2NH3(g)+CO2(g) NH2COONH4(s) + Q (Q>0 )
NH2COONH4(s) + Q (Q>0 )
制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。 当悬浮物较多时,停止制备。


注:四氯化碳与液体石蜡均为惰性介质。
(1)发生器用冰水冷却的原因是___________ _ _。
(2)液体石蜡 鼓泡瓶的作用是__ _____。
鼓泡瓶的作用是__ _____。
(3)从反应后的混合物中分离出产品的实验方法是_______(填写操作名称)。为了得到干燥产品,应采取的方法是________(填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
(4)尾气处理装置如右图所示。双通玻璃管的作用:________ ;
浓硫酸的作用: 、______________ _。
(5)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820 g,用足量石灰水充分处理 后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。则样品中氨基甲酸铵的物质的量分数为___________。
后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。则样品中氨基甲酸铵的物质的量分数为___________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省松原市高二下期末化学试卷(解析版) 题型:选择题
某兴趣小组探究SO2气体还原Fe3+的反应,他们使用的药品和装置如下图所示,下列说法不合理的是( )
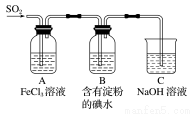
A.能表明I-的还原性弱 于SO2的现象是B中蓝色溶液褪色
于SO2的现象是B中蓝色溶液褪色
B.装置C的作用是吸收多余的SO2,防止污染空气
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2,产生白色沉淀
D.为了验证A中发生了氧化还原反应,加入酸性KMnO4溶液,紫红色褪去
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省松原市高二下期末化学试卷(解析版) 题型:选择题
下列实验叙述中正确的是( )
A. 用托盘天平称量2.50 g食盐
B. 用标准NaOH溶液滴定未知浓度盐酸,用去NaOH溶液20.50 mL
C. 用10 mL量筒量取8.25 mL盐酸
D. 用广泛pH试纸测得某溶液pH为3.0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江大庆铁人中学高二下期末化学试卷(解析版) 题型:选择题
300 mL Al2(SO4)3 溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol·L-1 Ba(OH)2 溶液300 mL,反应后溶液中SO42-的物质的量浓度为( )
A.0.1 mol·L-1 B.0.2 mol·L-1 C.0.3 mol·L-1 D.0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江大庆铁人中学高二下期末化学试卷(解析版) 题型:选择题
下列叙述中,正确的是:
A.10mL 质量分数为98%硫酸,用10mL 水稀释后,硫酸的质量分数小于49%
B.向两等份不饱和的烧碱溶液中分别加入一定量的氧化钠和过氧化钠,使溶液均恰好饱和, 则加入的氧化钠和过氧化钠的物质的量之比等于1:1(温度不变)
C.36.5 克HCl 溶解在1L 水中,所得溶液的密度为ρ g/ml,质量分数为ω ,物质的量溶液为c mol/L,则ω =36.5c/ρ
D.上述36.5g HCl 气体占有的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南师大附中高二下期末理综化学试卷(解析版) 题型:填空题
向2L密闭容器中通入amol 气体A和bmol气体B,在一 定条件下发生反应:xA(g)+yB(g)
定条件下发生反应:xA(g)+yB(g)  pC(g)+qD(g)。已知:平均反应速率VC=VA/2;反应2min 时,A的浓度减少了1/3,B的物质的量减少了
pC(g)+qD(g)。已知:平均反应速率VC=VA/2;反应2min 时,A的浓度减少了1/3,B的物质的量减少了 a/2mol,有a mol D生成。
a/2mol,有a mol D生成。
回答下列问题:
(1)反应2min内,VA = ,VB ;
(2)反应平衡时,D为 2amol,则B的转化率为 ;
(3)如果只升高反应温度,其他反应条件不变,平衡时D为 1.5a mol,则该反应的ΔH 0;(填“>”、“<”或“=”)
(4)如果其他条件不变,将容器的容积变为 1L,进行同样的实验,则与上述反应比较:
①反应速率 (填“增大”、“减小”或“不变”),理由是 ;
②平衡时反应物的转化率 (填“增大”、“减小”或“不变”),理由是 ;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东济南一中高二下期末化学试卷(解析版) 题型:选择题
下列说法正确的是
A.放热反应的反应速率一定大于吸热反应的反应速率
B.熔融状态下能导电的化合物一定含离子键
C.增大反应物浓度可加快反应速率,因此可用浓硫酸与锌反应增大生成氢气的速率
D.是否有丁达尔现象是胶体和溶液的本质区别
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com