
【题目】冰融化为水的过程的焓变和熵变正确的是( )
A. △H>0,△S>0 B. △H>0,△S<0
C. △H<0,△S>0 D. △H<0,△S<0
科目:高中化学 来源: 题型:
【题目】我国城市为了减少燃煤造成的大气污染,对作民用燃料的煤作了多方面的改进。
(1)为了除去煤中的含硫化合物,采用FeCl3脱硫,即用FeCl3溶液浸洗煤粉,发生如下反应:FeS2+14FeCl3+8H2O===2FeSO4+13FeCl2+16HCl。
①该反应中的氧化剂是________,若有1 mol FeS2被除去,则发生转移的电子的物质的量是________。
②为了充分利用Fe2+并减少酸(HCl)污染,本方法中可利用工业废铁屑和氯气让废液重新利用生成FeCl3。请写出这一过程中有关的离子方程式_____________________________、_________________________。
(2)某城市采用了以油制气代替煤作民用燃料的做法。油制气的主要成分是丙烷,请写出其燃烧的化学方程式:_______________________________。
(3)绿色能源是人类的理想能源,不会造成环境污染,下列能源属于绿色能源的是________。
A.氢能源 B.太阳能 C.风能 D.石油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种应用广泛的光敏材料光刻胶,其合成路线如下(部分试剂和产物已略去)

己知:I.
II.![]()
请回答下列问题
(1)A分子中所含官能团名称为______________________。
(2)乙炔和羧酸X加成生成E,E的核磁共振氢谱为三组峰,且峰面积比为3:2:1,E能发生水解反应,则E的结构简式为_____________________。
(3)F→G的条件和试剂是_____________________________。
(4)C物质不能发生的反应类型为_____________(填字母序号)。
a.加聚反应 b.缩聚反应 c.酯化反应 d. 还原反应
(5)B与Ag(NH3)2OH反应的化学方程式为:__________________________。
(6)与C具有相同官能团且含有苯环的同分异构体_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】公元前,有一位厨师不小心把刚熬好的羊油碰翻在灶坑旁,与草木灰混在一起,当他将羊油与草木灰的混合物用手捧出去后,洗手时发现手洗得特别干净。对此下列解释正确的是( )
A. 羊油是一种有机溶剂,溶解了厨师手上的油污
B. 草木灰呈碱性,与羊油发生了中和反应,除去油污
C. 羊油与草木灰中的物质发生了加成反应,除去油污
D. 羊油在碱性草木灰(K2CO3)的作用下发生了皂化反应,生成具有去油污能力的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如图所示的微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是

A. 断开K2,闭合K1时,总反应的离子方程式为:2H+ + 2Cl-![]() Cl2↑+H2↑
Cl2↑+H2↑
B. 断开K2,闭合K1时,石墨电极附近溶液变红
C. 断开K1,闭合K2时,铜电极上的电极反应为: Cl2+2e-=2Cl-
D. 断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3、NaHCO3是生活在常见的盐,某实验小组通过以下实验了探究这两种物质的性质(已知:Na2CO3、NaHCO3的水溶液均呈碱性;NaHCO3受热易分解生成Na2CO3、H2O和CO2)。
(1)称取两种固体各1g分别放入两支试管中,在各加入5mL水,振荡。固体成分溶解,并恢复至室温。
①发现Na2CO3完全溶解,而NaHCO3有剩余。由此得出结论:在相同温度下,________。
②向所得溶液中各滴入1~2滴酚酞溶液后,溶液均显________色。
(2)①取少量NaHCO3按下图装置进行实验。可观察到的现象是:大试管口有水珠生成,________________。
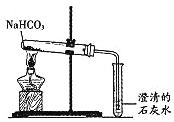
②用______________的方法除去混在Na2CO3粉末中少量的NaHCO3。
(3)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:
①称取mg样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,反应的化学方程式为_________________;证明反应后氯化钙有剩余的方法是______________________________。
③过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中Na2CO3的质量分数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A元素原子的核电荷数大于B元素原子的核电荷数,但两种元素的原子具有相同数目的电子层,A元素原子最外层电子数为B元素的两倍,A元素原子M层电子数为K层电子数的3倍,C元素原子的核电荷数是电子层数的4倍,其质子数为最外层电子数的6倍。请完成下列空白:
(1)A的原子结构示意图为____________;A元素的名称为____________。
(2)B的原子结构示意图为____________;B元素的名称为____________。
(3)C的离子结构示意图为____________;C元素的名称为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫分别通入下表所列溶液(装入试管)中至现象明显,如表实验报告记录的实验现象正确的是( )
石蕊试液 | 品红溶液 | 饱和硫化氢溶液 | 氯水 | |
A | 无色 | 无色 | 乳白色浑浊 | 无色 |
B | 红色 | 无色 | 黄色浑浊 | 无色 |
C | 红色 | 无色 | 乳白色浑浊 | 黄绿色 |
D | 无色 | 无色 | 乳白色浑浊 | 黄绿色 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是新型多功能水处理剂。其生产工艺如下:

回答下列问题:
(1)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl2反应生成NaClO3,写出温度较高时反应的离子方程式____________。
(2)在溶液I中加入NaOH固体的目的是_______(填字母)。
A.与反应液I中过量的Cl2继续反应,生成更多的NaClO
B.NaOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使NaClO3转化为NaClO
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。图1为不同的温度下,不同质量浓度的Fe(NO3)3对K2FeO4生成率的影响;图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4的生成率的影响。

工业生产中最佳温度为_______,此时Fe(NO3)3与NaClO两种溶液的最佳质量浓度之比为_____。
(4)反应③中的离子反应方程式为_________________;溶液Ⅱ中加入饱和KOH得到湿产品的原因是__________________。
(5)高铁酸钾作为水处理剂是能与水反应其离子反应是:4FeO42-+l0H2O=4Fe(OH)3(胶体)十3O2↑+8OH-。则其作为水处理剂的原理是:①_______________;②_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com