
 N2��+ 4H2O+Cl2��+2O2�����ų�����ΪQ�����жԴ˷�Ӧ�����д�����ǣ� ��
N2��+ 4H2O+Cl2��+2O2�����ų�����ΪQ�����жԴ˷�Ӧ�����д�����ǣ� ��| A����Ӧ���ڷֽⷴӦ |
| B��������Ӧ˲������������������ƶ�����ɻ����� |
| C����Ӧ�������仯��˵����Ҫ�ǻ�ѧ��ת��Ϊ���ܺͶ��� |
| D���ڷ�Ӧ�и������ֻ������������ |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��c(H��)�����¶ȵ����߶����� |
| B����35��ʱ��c(H��)��c(OH��) |
| C��ˮ�ĵ���Ȧ�(25��)����(35��) |
| D��ˮ�ĵ��������ȵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ڢۢ� | B���ݢޢߢ� | C���ۢݢޢߢ� | D���ۢܢݢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��HCl��NaOH��Ӧ���к��ȡ�H����57��3kJ/mol����H2SO4��Ca(OH)2��Ӧ���к���Ϊ2������57��3�� kJ/mol |
| B��CO(g)��ȼ������283��0 kJ/mol�����ʾCOȼ���ȵ��Ȼ�ѧ����ʽΪCO(g)��1/2O2(g)===CO2 (g)����H����283��0 kJ/mol |
| C����Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ |
| D��1 mol��ȼ��������̬�����������ų�����������ǵ�ȼ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ��ѧ�� | C��H | C=C | C��C | H��H |
| ����/kJ��mol��1 | 414��4 | 615��3 | 347��4 | 435��3 |
 2NH3(g) ��H=��92��4kJ/mol
2NH3(g) ��H=��92��4kJ/mol�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
 ��2���û���̿��ԭ��������������йط�ӦΪ��C(s)+2NO(g) N2(g)+CO2(g) ij�о�С����ij�ܱյ��������(��������������䣬��������������Բ���)�м���NO�������Ļ���̿������(T1��) �����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�
��2���û���̿��ԭ��������������йط�ӦΪ��C(s)+2NO(g) N2(g)+CO2(g) ij�о�С����ij�ܱյ��������(��������������䣬��������������Բ���)�м���NO�������Ļ���̿������(T1��) �����·�Ӧ����Ӧ���е���ͬʱ���ø����ʵ�Ũ�����£�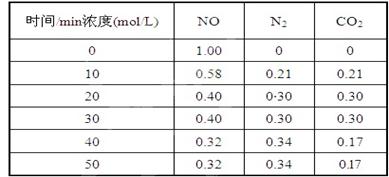
| A��������ѹǿ���ֲ��� | B��2v��(NO)=v��(N2) |
| C��������CO2������������� | D�����������ܶȱ��ֲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
| ���� | K+ | Na+ | N | S | N | Cl- |
| Ũ��/mol��L-1 | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
 O2(g) H2O(g) ��H="-241.8" kJ��mol-1 ��
O2(g) H2O(g) ��H="-241.8" kJ��mol-1 �� O2(g) CO(g)�� ��H="-110.5" kJ��mol-1 ��
O2(g) CO(g)�� ��H="-110.5" kJ��mol-1 �� 2NO(g)����H>0
2NO(g)����H>0�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ����һ | CO(g) +2H2(g)  CH3OH(g) CH3OH(g) |
| ������ | CO2(g) +3H2(g)  CH3OH(g) +H2O(g) CH3OH(g) +H2O(g) |

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com