
【题目】分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质有广泛用途。
(1)C8H8O3的某一同分异构体尼泊金酯的结构简式如图:
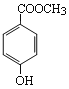
① 下列对尼泊金酯的判断正确的是______________。
a.能发生水解反应
b.能与FeCl3溶液发生显色反应
c.分子中所有原子都在同一平面上
d.能与浓溴水反应产生白色沉淀。
② 尼泊金酯与NaOH溶液在一定条件下反应的化学方程式是_________________________。
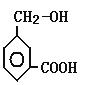
(2)C8H8O3的另一种同分异构体甲如图:
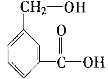
①请写出甲中所含官能团的名称________,________。
②甲在一定条件下跟Na反应的化学方程式是:__________。
③甲跟NaHCO3溶液反应的化学方程式是:____________
【答案】abd ![]() +2NaOH
+2NaOH![]()
![]() +CH3OH+H2O 羟基 羧基
+CH3OH+H2O 羟基 羧基 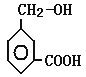 +2Na
+2Na![]()
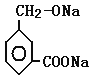 +H2
+H2![]()
 +NaHCO3
+NaHCO3![]()
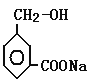 +H2O+CO2
+H2O+CO2![]()
【解析】
(1)尼泊金酯所含的官能团为酚羟基和酯基,按基团的结构、官能团的结构和性质判断说法是否正确并书写反应的化学方程式;
(2) 同分异构体甲所含的官能团为醇羟基和羧基,按官能团的性质书写反应的化学方程式;
(1)尼泊金酯的结构简式为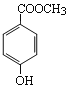 ,所含的官能团为酚羟基和酯基;
,所含的官能团为酚羟基和酯基;
①a.酯基能发生水解反应,a正确;
b.酚羟基能与FeCl3溶液发生显色反应,b正确;
c.分子中含有甲基,是四面体结构,故所有原子不可能都在同一平面上 ,c不正确;
d.酚羟基的邻位氢能与浓溴水发生取代反应产生白色沉淀,d正确;
答案为:abd;
② 尼泊金酯含有的酚羟基、酯基均能与NaOH溶液反应,在一定条件下反应的化学方程式是![]() +2NaOH
+2NaOH![]()
![]() +CH3OH+H2O;
+CH3OH+H2O;
答案为:![]() +2NaOH
+2NaOH![]()
![]() +CH3OH+H2O;
+CH3OH+H2O;
(2) ①同分异构体甲的结构简式为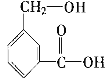 ,所含的官能团为醇羟基和羧基;
,所含的官能团为醇羟基和羧基;
答案为:羟基;羧基;
②甲所含的羟基和羧基均能在一定条件下跟Na反应,则化学方程式是 +2Na
+2Na![]()
 +H2
+H2![]() ;
;
答案为: +2Na
+2Na![]()
 +H2
+H2![]() ;
;
③甲所含的羧基能跟NaHCO3溶液反应,则化学方程式是: +NaHCO3
+NaHCO3![]()
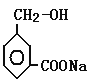 +H2O+CO2
+H2O+CO2![]() ;
;
答案为: +NaHCO3
+NaHCO3![]()
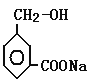 +H2O+CO2
+H2O+CO2![]() 。
。


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中,对于可逆反应:A(?)+3B(?)![]() 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是

A. 若正反应方向△H<0,则T1>T2 B. 压强增大时,混合气体的平均相对分子质量减小
C. A一定为气体 D. B一定为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰丙酮铜是金属有机化合物中一种重要的化合物,广泛应用于化工、石油、制药、电子、材料、机械等领域。实验室制备原理如下:
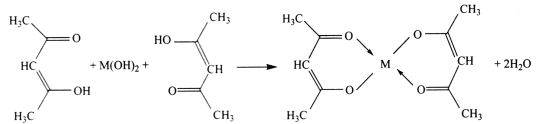
实验步骤:
(1)制取氢氧化铜(II)
分别称取4.000g(0.1mol)氢氧化钠、8.000g(0.05mol)无水硫酸铜于250mL、100mL烧杯中,加入适量的蒸馏水使其溶解,然后将硫酸铜溶液倒入氢氧化钠溶液中,摇匀,使反应完全,再将沉淀进行抽滤。
(2)制备乙酰丙酮铜(II)
称取0.1960g(2mmol)新制的氢氧化铜于100mL仪器a中,在氮气保护下加入少量的四氢呋喃,并进行搅拌,约五分钟之后,加入0.4000g(4mmol)乙酰丙酮,补充四氢呋喃约30mL,在50℃下加热回流约2h,然后冷却至室温,转移到锥形瓶中,用薄膜封口,放置4~5天,得到蓝色针状晶体。
已知:
I.氢氧化铜(II)分解温度为60℃。
II.四氢呋喃易挥发,沸点66℃,储存时应隔绝空气,否则易被氧化成过氧化物。
III.乙酰丙酮铜(II)是一种蓝色针状晶体,难溶于水,微溶于乙醇,易溶于苯、氯仿、四氯化碳。66.66kPa压力下,78℃升华。
回答下列问题:
(1)制取氢氧化铜(II)时采用抽滤的方式进行,已知抽滤装置如图所示,抽滤与常规过滤相比其优点是____________________。
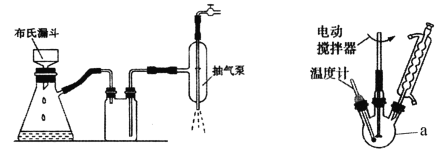
(2)制备乙酰丙酮铜(II)时采用氮气保护的目的________________,加入四氢呋喃的作用是__________________。
(3)加热回流简易装置如图(加热部分省略)所示,仪器a的名称是_______________,加热回流时采用球形冷凝管而不选用直形冷凝管的原因是________________。加热方式宜采用_______________。在50℃下加热回流的原因除防止四氢呋喃挥发外,还有可能的原因是_____________(用化学方程式表示)。
(4)若要纯化乙酰丙酮铜晶体,可以采用的实验方法是___________。若纯化后蓝色针状晶体的质量为0.3630g(乙酰丙酮铜的相对分子质量为262),则产率为________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用![]() 、
、![]() 可以制备含有
可以制备含有![]() 的
的![]() 悬浊液,该悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米
悬浊液,该悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米![]() 。
。
(1)基态![]() 的核外电子排布式为__________。
的核外电子排布式为__________。
(2)与![]() 互为等电子体的一种分子为________(填化学式)。
互为等电子体的一种分子为________(填化学式)。
(3)![]() 与
与![]() 反应能生成
反应能生成![]() ,
,![]() 中的配位原子为________(填元素符号)。
中的配位原子为________(填元素符号)。
(4)乙醛(![]() )中碳原子的轨道杂化类型是_________;
)中碳原子的轨道杂化类型是_________;![]() 中含有
中含有![]() 键的数目为________
键的数目为________![]() 。
。
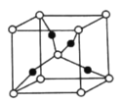
(5)一个![]() 晶胞(见图)中,
晶胞(见图)中,![]() 原子的数目为________。
原子的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物Targretin(F)能治疗顽固性皮肤T细胞淋巴瘤,其合成路线如图所示:
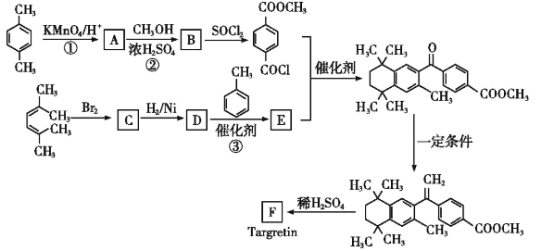
已知:
ⅰ.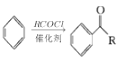
ⅱ.![]()
ⅲ.RCOOH![]() RCOCl(R表示烃基)
RCOCl(R表示烃基)
(1)反应①的反应类型是__。
(2)反应②的化学方程式:__。
(3)C的核磁共振氢谱图中有__个峰。
(4)反应③的化学方程式:__。
(5)F的分子式是C24H28O2。F中含有的官能团:__。
(6)写出满足下列条件A的两种同分异构体的结构简式(不考虑-O-O-或![]() 结构):__。
结构):__。
a.苯环上的一氯代物有两种
b.既能发生银镜反应又能发生水解反应
(7)已知:![]() (R、R′为烃基)。以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成
(R、R′为烃基)。以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成![]() ,写出合成路线__(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件。
,写出合成路线__(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用如图所示装置制取溴苯和溴乙烷.已知溴乙烷为无色液体,难溶于水,沸点为38.4℃,熔点为-190℃,密度为1.46gcm-3。
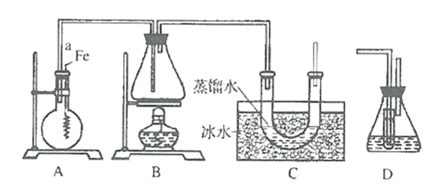
主要实验步骤如下:
①检查装置的气密性后,向圆底烧瓶中加入一定量的苯和液溴。
②向锥形瓶中加入乙醇和浓H2SO4的混合液至浸没进气导管口。
③将A装置中的纯铁丝小心向下插入混合液中。
④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10min。
请填写下列空白:
(1)写出A装置中制取溴苯的化学方程式__。
(2)导管a的作用是__。
(3)C装置中U型管内部用蒸馏水封住管底的作用是__。
(4)反应完毕后,U型管内液体分层,溴乙烷在__层(填:上或下)。
(5)步骤④中__(填“能”“否”)用大火加热,理由是__。
(6)为探究溴和苯的上述反应是取代反应而不是加成反应,用装置D代替装置B、C直接与A相连重新操作实验。
①装置D中小试管内装有CCl4,其主要作用是__。
②锥形瓶中装有水,反应后向锥形瓶的水溶液中滴加硝酸银溶液,若有__产生,证明该反应为取代反应。
(7)要检验某溴乙烷中的溴元素,正确的实验方法是:向盛有适量溴乙烷的试管中__。
A.加入新制的氯水振荡,再加入少量CCl4振荡,观察下层是否变为橙红色
B.滴入硝酸银溶液,再加入稀硝酸使溶液呈酸性,观察有无浅黄色沉淀生成
C.加入NaOH溶液共热,冷却后加入硝酸银溶液,观察有无浅黄色沉淀生成
D.加入NaOH溶液共热,冷却后加入稀硝酸使溶液呈酸性,再滴入硝酸银溶液,观察是否有浅黄色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值。
(1)在基态Ti原子中,核外存在_____对自旋相反的电子,核外电子占据最高能层的符号是___,占据该能层电子的电子云轮廓图形状为____。
(2)TiCl3 可用作烯烃定向聚合的催化剂,例如丙烯用三乙基铝和三氯化钛做催化剂时,可以发生下列聚合反应:nCH3CH=CH2 ![]()
![]() ,该反应中涉及的物质中碳原子的杂化轨道类型有_______;反应中涉及的元素中电负性最大的是______。 三乙基铝是一种易燃物质,在氧气中三乙基铝完全燃烧所得产物中分子的立体构型是直线形的是__________。
,该反应中涉及的物质中碳原子的杂化轨道类型有_______;反应中涉及的元素中电负性最大的是______。 三乙基铝是一种易燃物质,在氧气中三乙基铝完全燃烧所得产物中分子的立体构型是直线形的是__________。
(3)[TiO(H2O2)2]2+配离子呈黄色。提供中心原子孤电子对的成键原子是_____(填元素符号);配体之一H2O2分子中氧原子的价层电子对互斥模型是___。
(4)科学家通过X射线探明一种氮化钛的晶体与NaCl的晶体结构相似。氮化钛熔点(2950℃)比氯化钠的高,主要原因是________________。
(5)有一种氮化钛晶体的晶胞如图所示,该晶体中Ti原子周围与Ti原子距离最近且相等的N原子的个数为_____。已知晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,则晶胞边长为____cm(用含ρ、NA的式子表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸锂电池应用广泛, 电池放电后负极材料主要含有Li4Ti5O12、 铝箔及少量Fe, 可通过下列工艺流程回收钛、 锂。回答下列问题:

(1) Li4Ti5O12中, Ti元素的化合价为___, 滤液1中含金属的阴离子是___(填离子符号)。
(2) 酸浸时 Li4Ti5O12发生的反应是: Li4Ti5O12+7H2SO4+5H2O2=2Li2SO4+5[TiO(H2O2)]SO4+7H2O, 该反应是否属于氧化还原反应?___(填 “是” 或 “否”); 滤渣1是___。
(3) 向[TiO(H2O2)]SO4溶液中加入Na2SO3溶液发生反应的离子方程式为___。
(4) 向TiOSO4溶液中通入NH3发生反应的离子方程式为___。
(5) 沉淀TiO(OH)2用蒸馏水洗涤的目的是___。
(6) 萃取时, 温度对萃取率的影响如图所示。由图分析知实验时选择在常温下进行即可, 理由是__。

(7)“萃取” 和 “反萃取” 可简单表示为:[TiO(H2O2)]2++2(HA)2![]() [TiO(H2O2)](HA2)2+2H+,则反萃取过程中加入的试剂X是___。
[TiO(H2O2)](HA2)2+2H+,则反萃取过程中加入的试剂X是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用![]() 和
和![]() 制备
制备![]() 的原理为:
的原理为:
①![]()
②![]()
已知:A、B均为有机物,两个反应均能自发进行;NA代表阿伏加德罗常数。下列说法正确的是
A.B为![]() 和
和![]() 制备
制备![]() 的催化剂
的催化剂
B.1mol![]() 与足量的B在一定条件下发生反应②,共转移2NA个电子
与足量的B在一定条件下发生反应②,共转移2NA个电子
C.反应①的反应物的总能量大于产物的总能量
D.标准状况下,22.4L![]() 含NA个分子
含NA个分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com