
| A. | 乙酸 | B. | 苯酚 | C. | 水 | D. | 乙醇 |
分析 根据酸性越强电离生成H+越容易,则最难电离出H+的是酸性最弱的物质或非电解质.
解答 解:A.CH3COOH是一种弱酸,CH3COOH?CH3COO-+H+在水溶液中能电离出H+;
B.C6H5ONa+CH3COOH→C6H6OH+CH3COONa,乙酸电离生成H+比苯酚强,但苯酚显弱酸性,电离出氢离子的能力比水强;
C.水属于极弱电解质,能微弱电离生成H+;
D.C2H5OH属于非电解质,在水中不电离,则不会电离出H+;
四种物质的酸性关系为CH3COOH>C6H6OH>H2O>C2H5OH,即最难电离出H+的是C2H5OH,
故选D.
点评 本题较简单,注重对学生基础知识的考查,明确酸性强弱与电离生成H+的关系是解答本题的关键.


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:选择题
| A. | 2Na+2H2O?2NaOH+H2↑ | B. | Cl2+H2O?HCl+HClO | ||
| C. | NH3•H2O?NH3+H2O | D. | N2+3H2$?_{高温高压}^{催化剂}$2NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
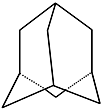 金刚烷的结构如图所示,它可看作是由四个等同的六元环组成的空间构型.
金刚烷的结构如图所示,它可看作是由四个等同的六元环组成的空间构型.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 现使用酸碱中和滴定法测定市售白醋(CH3COOH)的总酸量(g/100mL).
现使用酸碱中和滴定法测定市售白醋(CH3COOH)的总酸量(g/100mL).| 滴定次数 | 1 | 2 | 3 | 4 |
| V(样品) (mL) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) (mL) | 15.95 | 15.00 | 15.05 | 14.95 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com