
【题目】用惰性电极电解一定浓度的CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1molCu(OH)2后恰好恢复到电解前的浓度和pH.则下列说法正确的是( )
A.电解过程中阴极没有气体生成
B.电解过程中转移的电子的物质的量为0.4 mol
C.原CuSO4溶液的浓度为0.1 molL﹣1
D.电解过程中阳极收集到的气体体积为1.12 L(标况下)
【答案】B
【解析】解:Cu(OH)2从组成上可看成CuOH2O,加入0.1 mol Cu(OH)2后恰好恢复到电解前的浓度和pH,即电解生成了0.1 mol H2SO4 , 并电解了0.1 mol H2O,由电解的总反应式:
2H2O | + | 2CuSO4 |
| 2Cu | + | O2↑ | + | 2H2SO4 | 转移电子 |
2mol | 2mol | 1mol | 4mol | ||||||
0.1mol | 0.1mol | 0.05mol | 0.2mol |
2H2O |
| 2H2↑ | + | O2↑ | 转移电子 |
2mol | 2mol | 1mol | 4mol | ||
0.1mol | 0.1mol | 0.05mol | 0.2mol |
A、根据以上分析,阴极有氢气放出,故A错误;
B、根据以上分析计算,电解过程中共转移电子为0.4 mol,故B正确;
C、没有体积无法计算,故C错误;
D、根据以上分析,阳极收集到的气体体积为(0.05+0.05)×22.4=2.24L,故D错误;
故选:B.


科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是短周期的5种元素,它们的原子序数依次增大.A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳.
(1)请写出B、D元素的名称:B , D .
(2)画出C元素的离子结构示意图 .
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式 .
(4)A、B、C三种元素形成的化合物的电子式为 , 所含的化学键类型为 .
(5)A、E形成化合物的结构式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代许多文献中记录的现象都与化学有关,下列有关古代文献的说法,错误的是( )
A. “青蒿一握,以水二升渍,绞取汁”,不涉及化学变化
B. “曾青得铁则化为铜”指铜可以采用湿法冶炼
C. “丹砂(HgS)烧之成水银,积之又成丹砂”可知HgS受热会分解
D. “日照香炉生紫烟,遥看瀑布挂前川”,“紫烟”指“香炉”中碘升华的现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中,互为同位素的是 , 互为同素异形体的是 , 互为同系物的是 , 互为同分异构体的是 .
①金刚石与石墨
②12C与14C
③ ![]() 与
与 ![]()
④ 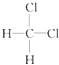 与
与 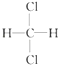
⑤ 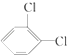 与
与 ![]()
⑥ 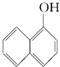 与
与 ![]()
⑦CH4与C(CH3)4 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语书写正确的是( )
A.氯原子的结构示意图: ![]()
B.作为相对原子质量测定标准的碳核素: ![]() ?C
?C
C.氯化镁的电子式: ![]()
D.用电子式表示氯化氢分子的形成过程: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品的主要成分大都是有机化合物.以下食品中的有机成分属于高分子化合物的是( )
A.食醋中含有的醋酸
B.酒中含有的酒精
C.谷类中含有的淀粉
D.植物油、动物脂肪中含有的油脂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素在化学中有着极为广泛的应用。
Ⅰ. 由于氟的特殊化学性质,它和其他卤素在单质及化合物的制备与性质上存在较明显的差异。
(1)化学家研究发现,SbF5能与[MnF6]2-离子反应得到MnF4,SbF5转化成稳定离子[SbF6]-的盐。而MnF4很不稳定,受热易分解为MnF3和F2。根据以上研究写出以K2MnF6和SbF5为原料,在423 K 的温度下制备F2的化学方程式:________________________________________________。
(2)现代工业以电解熔融的氟氢化钾(KHF2)和氟化氢(HF)混合物制备氟单质,电解制氟装置如图所示。

电解制氟时,要用镍铜合金隔板将两种气体产物严格分开的原因是______________________。
(3)HF的水溶液是氢氟酸,能用于蚀刻玻璃,其化学反应方程式为: ____________________。
Ⅱ. 实验室常用高锰酸钾固体与浓盐酸反应制备氯气。将0.08mol KMnO4固体加热一段时间后,收集到a molO2;向反应后残留的固体中加入足量的浓盐酸,又收集到b mol Cl2,此时Mn元素全部以Mn2+的形式存在于溶液中。
(1)请根据上述描述写出K2MnO4与浓盐酸反应制氯气的离子反应方程式:__________________。
(2)通过上述文字中提供的数据计算出a+b的范围为_____________________。
Ⅲ. ClO2可替代Cl2作为自来水消毒剂。常用 “有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。则ClO2的有效氯含量为__________。(计算结果保留两位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com