
| A. | Ag+ NH3 | B. | Cu2+ NH3 | C. | H+ H2O | D. | Ag+ CH4 |
分析 含有孤电子对和含有空轨道的原子之间能形成配位键,配位键属于共价键,根据配位键形成的条件分析,一方要提供空轨道,另一方提供孤电子对,据此答题.
解答 解:A.Ag+有空轨道,NH3中的氮原子上的孤电子对,可以形成配位键,故A不选;
B.Cu2+有空轨道,NH3中的氮原子上的孤电子对,可以形成配位键,故B不选;
C.水分子中的O原子含有孤电子对,H+有空轨道,所以能形成配位键,故C不选;
D.Ag+有空轨道,Ag+、CH4两种微粒都没有孤电子对,所以不能形成配位键,故D选;
故选D.
点评 本题考查了配位键,明确配位键的形成条件是解本题关键,熟悉常见微粒中是否含有孤电子对或空轨道,只要符合配位键的形成条件就能形成配位键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

 ..
..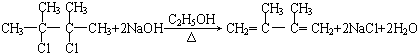 .
. ;②、⑥的反应类型依次是消去反应、取代反应.
;②、⑥的反应类型依次是消去反应、取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度 | B. | 加入适当的催化剂 | ||
| C. | 充入He(g),使体系压强增大 | D. | 再向容器中通入2molO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (2)冷凝管中的冷凝水的流向应是B
(2)冷凝管中的冷凝水的流向应是B查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,28.6gNa2CO3•10H2O晶体中含的CO32-数目为0.1NA | |
| B. | 78.0g苯中σ键的数目为6NA | |
| C. | 标准状况下22.4LCl2通入足量的水中,反应转移的电子总数目为NA | |
| D. | 常温,pH=13的NaOH溶液中含有O.1NA个Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol乙醇含有共价键的数目为6NA | |
| B. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA | |
| C. | 在标准状况下22.4L己烷完全燃烧,生成CO2分子数为6NA | |
| D. | 0.2mol甘油与足量的钠反应生成6.72L氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z可以电离 | B. | Z的电子式为 | C. | X形成+2价阳离子 | D. | Z可以表示为XY2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com