下列液体均处于25℃,有关叙述正确的是( )
A.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐
B.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-)
C.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同
D.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍
【答案】
分析:A、室温下,溶液呈酸性,呈酸性的原因可能是酸电离或强酸弱碱盐水解或弱酸弱碱盐水解.
B、先根据溶液的酸碱性判断c(H
+)、c(OH
-)的大小,然后利用电荷守恒判断c(Na
+)、c(CH
3COO
-)的大小.
C、根据溶度积常数判断.
D、把PH值换算成氢离子浓度,然后求出比值来判断.
解答:解:A、常温下,某物质的溶液pH<7,说明溶液呈酸性,可以是酸的溶液,酸电离使溶液呈酸性;也可以是盐的溶液,盐类水解使溶液呈酸性,盐可以是强酸弱碱盐或弱酸弱碱盐,也可能是强酸的酸式盐,故A错
B、CH
3COOH与CH
3COONa混合溶液中,存在离子有:Na
+、H
+、CH
3COO
-、OH
-,由电荷守恒:c(Na
+)+c(H
+)=c(CH
3COO
-)+c(OH
-),因为PH=5.6,溶液呈酸性,c(H
+)>c(OH
-),所以,c(Na
+)<c(CH
3COO
-),故B错
C、一定温度下AgCl的溶度积Ksp(AgCl)=c(Ag
+)?c(Cl
-)是定值,c(Ag
+)=
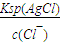
,同浓度的CaCl
2和NaCl溶液中,Cl
-浓度前者是后者的2倍,所以,AgCl在NaCl溶液中的溶解度更大.故C错
D、pH=4.5的番茄汁中c(H
+)=10
-4.5,pH=6.5的牛奶中c(H
+)=10
-6.5,
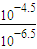
=100,故D对
故选D
点评:利用电荷守恒是解本题的关键.

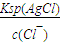 ,同浓度的CaCl2和NaCl溶液中,Cl-浓度前者是后者的2倍,所以,AgCl在NaCl溶液中的溶解度更大.故C错
,同浓度的CaCl2和NaCl溶液中,Cl-浓度前者是后者的2倍,所以,AgCl在NaCl溶液中的溶解度更大.故C错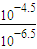 =100,故D对
=100,故D对

 名校课堂系列答案
名校课堂系列答案