
��������������������λ��ѧ�����о������ӻ����������ϳɡ����2016��ŵ������ѧ����������һ�ַ��ӻ����ġ����ӡ����ϳ�����Ļ���ԭ����CH2C12����ϩ���촼����������˵������ȷ����

A. CH2C12������ͬ���칹��
B. ��ϩ��ʹ��ˮ��ɫ
C. �촼��һ���������������ᷢ��������Ӧ
D. �����������������������»ᷢ���ӳɷ�Ӧ���ɻ�����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ����3�¸߿�ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���б仯�����У�ԭ���ʷ����ڹ��ۼ����ƻ���ͬʱ�����Ӽ��γɵ��� ( )
A. �����NaOH��Һ��� B. �Ȼ�������ˮ
C. �廯�������백��������Ӧ D. п��ϡ���ᷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ�ɶ��и�������ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��������泥�H2NCOONH4����һ���ֽ⡢��ˮ��İ�ɫ���壬�����ڻ��ʡ�������ϴ�Ӽ��ȡ�ij��ѧ��ȤС��ģ�ҵԭ���Ʊ���������泥�
��Ӧʽ��2NH3 (g)+CO2 (g)  H2NCOONH4 ��H <0
H2NCOONH4 ��H <0
��1�����ʹ����ͼ��ʾ��װ����ȡNH3������ѡ����Լ���_____________��
��2���Ʊ���������淋�װ������ͼ���Ѱ��Ͷ�����̼ͨ�����Ȼ�̼�У����Ͻ����ϣ����ɵİ��������С�������������Ȼ�̼�У���������϶�ʱ��ֹͣ�Ʊ�����ע�����Ȼ�̼��Һ��ʯ����Ϊ���Խ��ʡ���
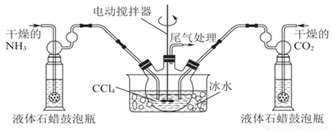
�ٷ������ñ�ˮ��ȴ��ԭ����_______��Һ��ʯ������ƿ��������__________��������Ӧ������������_______________��
�ڴӷ�Ӧ��Ļ�����й��˷������Ʒ��Ϊ�˵õ������Ʒ��Ӧ��ȡ�ķ�����_____ (ѡ����ţ�
a����ѹ���Ⱥ�� b����ѹ���Ⱥ�� c�����40�����º��
��3��β������Ⱦ������________��Һ���մ�����
��4��ȡ�ֱ��ʶ�����̼����淋İ��������Ǯ��Ʒ1.1730g��������ʯ��ˮ��ִ�����ʹ̼Ԫ����ȫת��Ϊ̼��ƣ����ˡ�ϴ�ӡ�����������Ϊ1.500g����Ʒ�а�������淋���������Ϊ__________��[��֪Mr(H2NCOONH4)=78, Mr(NH4HCO3)=79, Mr(CaCO3)=100]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ̩���и�����һ�ָ�ϰ������⣨һģ�������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ç������ijЩ�ߵ�ֲ�����е�֬��״�л��᳣������һ����ṹ��ʽ��ͼ��ʾ������˵����ȷ����
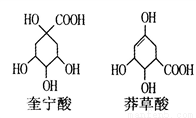
A. ��������ç���ụΪͬ���칹��
B. �����Ậ�еĹ�������ȫ��ͬ
C. ��������ܷ����ӳɷ�Ӧ���ۺϷ�Ӧ��ȡ����Ӧ
D. �����ʵ����Ŀ������ç����ֱ�������Na��Ӧ��ͬ��ͬѹ�²���H2�������Ϊ5��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�����и����ڶ��δ��������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
���շۣ�Na2S2O4���м�ǿ�Ļ�ԭ�ԣ�����ˮ��ʪ������ֽⷢ�ȣ����ڼ��Ի����½��ȶ����ش��������⣺
(1)����������Ʊ�
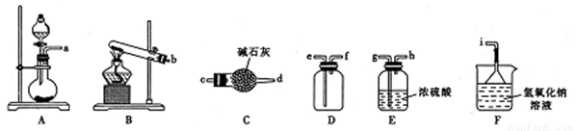
�ٶ�������ķ���װ�ÿ���ѡ����ͼ�е�_____________�����д��ĸ������Ӧ�Ļ�ѧ����ʽΪ______________________��
�����ռ�һƿ����Ķ�������ѡ����ͼ�е�װ�ã���ӿڵ�����˳��Ϊ����װ�á�__________________����______��______�� ____________����������������Сд��ĸ��ʾ��
(2)���շ۵��Ʊ�
��35-45���£���SO2����ͨ��п��һˮ����Һ�У���ͼ����ʹ֮������Ӧ����ZnS2O4������Ӧ��ȫ�����ߺ���ˮԡװ�ò���ȴ�����£���������ƿ�м���18%��NaOH��Һ��ʹ֮������Ӧ����Na2S2O4��Zn(OH)2����һϵ�в�����õ���ˮNa2S2O4��Ʒ��
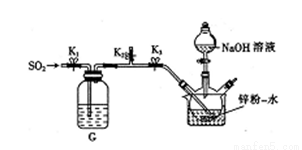
��ʵ�鿪ʼʱ��Ӧ�ȹر�ֹˮ��K3����K1��K2��ͨ��һ��ʱ��SO2����ԭ����__________��
��ͨ���۲�_________________������ֹˮ��K1������SO2�����١�
����ZnS2O4����Na2S2O4�Ļ�ѧ����ʽΪ_____________��
(3)��ȡ2.0gNa2S2O4��Ʒ������ˮ�У����100mL����Һ��ȡ��10mL����Һ���Թ��У���0 .10 mol/L��KMnO4��Һ�ζ����ζ����յ�ʱ����ΪNa2SO4��MnSO4�����ظ���������2�Σ�ƽ��������Һ12.00mL�������Ʒ��Na2S2O4����������Ϊ_______�����ʲ����뷴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�켪��ʡ�����и�����ѧ�ڵڶ�������������ۻ�ѧ�Ծ��������棩 ���ͣ������
2016��9�£����Ǹ���1�š��й���̨��Ĭ�ƶ�����վMFC30��ʽ������MFC30�ǻ��ڼ״���������ȼ�ϵ�ط��缼����
��1���״����ⷽʽ��Ҫ���������֣���Ӧ��״�ˮ�����������⣺CH3OH(g)+H2O(g)  CO2(g)+3H2(g) ��H1=+49.4 kJ/mol��Ӧ��״��ֽ����⣺CH3OH(g)
CO2(g)+3H2(g) ��H1=+49.4 kJ/mol��Ӧ��״��ֽ����⣺CH3OH(g) CO(g)+2H2(g) ��H2=+90.6 kJ/mol��Ӧ����̬�״�������������ͬʱ���ɶ�����̼��������
CO(g)+2H2(g) ��H2=+90.6 kJ/mol��Ӧ����̬�״�������������ͬʱ���ɶ�����̼��������
����֪CO��ȼ����Ϊ283.0 kJ/mol����Ӧ����Ȼ�ѧ��Ӧ����ʽΪ____________��
�ڸ��������ⷽʽ�У������ļ״��������������Ƿ�Ӧ____________��(�����������
��2��ʵ����ģ�ⷴӦ��״�ˮ��������������۲죬�ϳ������n(CH3OH): n(H2O)=1��1ʱ����ϵ�м״���ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��

�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪ____________________��
�ڵ��¶�Ϊ250�桢ѹǿΪP2ʱ����Ӧ��ƽ��ʱH2���������Ϊ____________��
��ͼ�е�ѹǿ��С�����˳����____________��
��3��MFC30ȼ�ϵ��������Ϊȼ�ϣ�Li2CO3��K2CO3��ϵ�̼����Ϊ����ʵĸ�����ȼ�ϵ�أ��为���ĵ缫��ӦʽΪ____________��������ͨ�������Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�켪��ʡ�����и�����ѧ�ڵڶ�������������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
W��X��Y��Z��Ϊ������Ԫ�أ�ԭ��������������W��ԭ�Ӻ��������������Ǵ�����������2����X-��Y+������ͬ�ĵ��Ӳ�ṹ��Z�������Ӳ��ܷ���ˮ�ⷴӦ������˵������ȷ���ǣ� ��
A. ԭ�Ӱ뾶�� Y��Z��X��W
B. ���⻯����ȶ��ԣ�W��Z��X
C. Z��W��Y�γɵĻ������У��仯ѧ�����Ͳ���ͬ
D. ����������ˮ��������ԣ�W��Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ���������е�ʮ��У�ص���ѧ������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A. �Ȼ�������Һ��ͨ��������Fe2++Cl2=Fe3++2Cl-
B. ������������������ͨ���䰱ˮ�У�SO2+NH3��H2O=HSO3-+NH4+
C. �������������м�������ϡ���Fe(OH)2+2H+=Fe2++2H2O
D. ��������Һ�������Һ��ϣ�SiO32-+2H+=H2SiO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ��ɽ�и����ڶ��ε����о����������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
̼��������FeCO3������þ�����Ҫ�ɷ֣���FeCO3���ȵ�200�濪ʼ�ֽ�ΪFeO��CO2�����ڿ����и�������FeCO3����Fe2O3��
I����֪25�棬101kPaʱ��4Fe(s)+3O2(g)=2Fe2O3(s) ��H=-1648kJ/mol
C(s)+ O2(g)=CO2(g) ��H=-393 kJ/mol 2FeCO3(s)=2Fe(s)+ 3O2(g) ��H=+148OkJ/mol
��1����д��FeCO3�ڿ�������������Fe2O3���Ȼ�ѧ����ʽ_______��
�����ɵ�FeO��Fe2O3��һ�������±���ԭΪ��������
��2���ݱ���һ��������Fe2O3�ɱ����黹ԭΪ���������Ľ��������䷴ӦΪ��
Fe2O3(s)+3CH4(g)=2Fe(s)+3CO(g)+6H2(g) ��H>0
�� ԭ������Ϊ26����Ԫ��λ��Ԫ�����ڱ��ĵ�_______���ڡ�
�ڷ�Ӧ��5L���ܱ������н��У�2min��ﵽƽ�⣬���Fe2O3�ڷ�Ӧ����������4.8g����ö�ʱ������H2�����ƽ����Ӧ����Ϊ____________��
�۽�һ������Fe2O3(s)��һ������CH4(g)���ں��º�ѹ�����У���һ�������·�Ӧ���ܱ����÷�Ӧ�ﵽƽ��״̬����___________��
a.CH4��ת���ʵ���CO�IJ��� b����������ƽ����Է�����������
c.v��(CO)��v��(H2)=1:2 d.���������������
��3��FeO����CO���л�ԭ����֪��t��ʱ��FeO(s)+CO(g) Fe(s)+CO2(g)��K=0.5������1L�ܱ������м���0.04mol FeO(s)����ͨ��xmolCO��t��ʱ��Ӧ�ﵽƽ�⡣��ʱFeO(s)��ת����Ϊ50%����x=_______��
Fe(s)+CO2(g)��K=0.5������1L�ܱ������м���0.04mol FeO(s)����ͨ��xmolCO��t��ʱ��Ӧ�ﵽƽ�⡣��ʱFeO(s)��ת����Ϊ50%����x=_______��
��. Fe2O3���������Ʊ�FeCl3��FeCl3��ˮ��Һ�е�ˮ���������
Fe3++H2O Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++ H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)2++ H2O Fe (OH)3+H+ K3
Fe (OH)3+H+ K3
��4������ˮ�ⷴӦ��ƽ�ⳣЧK1��K2��K3�ɴ�С��˳����_______��ͨ����������������ˮ�����ۺ����ɾۺ�������ӷ���ʽΪ��xFe3++yH2O===Fex(OH)y(3x-y)++yH+
��ʹƽ�������ƶ��ɲ��õķ�����__________������ĸ��
a����ˮϡ�� b����������NaCl���� c������ d����������Na2CO3����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com