
| A.大气污染主要指CO、SO2、氮氧化物以及粉尘等 |
| B.氮氧化物是造成光化学烟雾的主要原因 |
| C.臭氧可以杀菌消毒,空气中的臭氧含量越高,对人体健康越有利 |
| D.酸雨通常是指pH在5.6以下的降水 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| AgNO3溶液 | 蓝色石蕊试纸 | Na2CO3溶液 | |
| A | 产生沉淀 | 变红后无现象 | 有气泡 |
| B | 无明显现象 | 变红后无现象 | 产生沉淀 |
| C | 产生沉淀 | 先变红后褪色 | 有气泡 |
| D | 产生沉淀 | 先变红后褪色 | 产生沉淀 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | SiO2可以和NaOH溶液及HF溶液反应 | SiO2属于两性氧化性 |
| D | 将SO2通入溴水中,酸性高锰酸钾溶液褪色 | SO2具有漂白性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碘酒是指单质碘的乙醇溶液 |
| B.84消毒液的有效成分是NaClO |
| C.浓硫酸可刻蚀石英制艺术品 |
| D.装饰材料释放的甲醛会造成污染 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
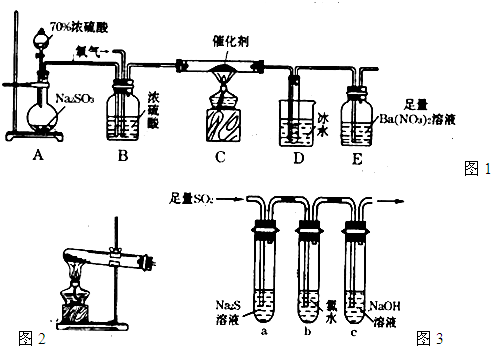
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验事实 | 解释或结论 |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,溶液褪色 | SO2具有漂白性 |
| B | 将BaSO4浸泡在饱和Na2CO3溶液中,部分BaSO4转化为BaCO3 | Ksp(BaSO4)>Ksp(BaCO3) |
| C | 某钾盐溶于盐酸,产生无色无味气体,该气体通入澄清石灰水,有白色沉淀出现 | 该钾盐可能是K2CO3 |
| D | NaI溶液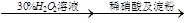 溶液变蓝色 溶液变蓝色 | 酸性条件下H2O2的氧化性比I2强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 气体X | 液体Y | 试管内现象 |
| A | NH3 | 滴有酚酞的水溶液 | 充满红色溶液 |
| B | NO2 | 水 | 充满无色溶液 |
| C | SO2 | 滴有品红的水溶液 | 无明显现象 |
| D | C2H4 | 酸性KMnO4溶液 | 无明显现象 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
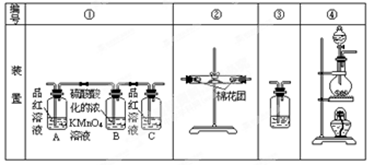
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com