
(1)该生的操作方法是否正确?
(2)如不正确请说明理由,并分析是否一定有误差产生。
(3)若用此法分别测定c(H+)相等的H2SO4和H3PO4溶液的pH,结果会怎样?
思路解析:(1)pH试纸用于测定溶液的pH,不能将其润湿,否则,测得的是稀释后溶液的pH,引起误差。
(2)pH试纸润湿是否会引起测定误差,关键是取决于待测溶液的性质,若待测液为中性溶液,润湿后c(H+)不变,不会引起误差;若待测液为碱溶液或酸溶液,由于润湿会引起c(OH-)或c(H+)变化,从而引起pH变化,测定会有误差。
(3)由于在稀释过程中,H3PO4继续电离产生H+,使得该溶液中c(H+)较H2SO4溶液中的c(H+)大,故测H3PO4的pH较H2SO4小。
答案:(1)不正确。
(2)若溶液不显中性,则H+或OH-被稀释,测出的值不为原溶液的pH;不一定有误差,当溶液为中性时则不产生误差。
(3)测得H3PO4的pH较H2SO4小。


科目:高中化学 来源: 题型:阅读理解
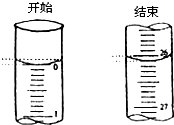 某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定次数 | 待测氢氧化钠 溶液的体积/mL |
0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:
①该学生的操作是__________(填“正确的”或“错误的”),其理由是___________________。
②如不正确请说明理由,同时请分析是否一定有误差?答_____________________。
③若用此法分别测定[H+]相等的盐酸和醋酸溶液的pH,误差较大的是_________________,原因是_____________________________________________。
(2)若以铁棒、碳棒、导线和氯化铁溶液为用品设计原电池。
负极材料为_______________,电极反应式为_______________;
正极材料为_______________,电极反应式为_______________;
电池总反应式为______________________________________________________。
(3)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知:0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256.652 kJ的热量。
①反应的热化学方程式为__________________。
②又已知H2O(l)![]() H2O(g) ΔH=+44 kJ·mol-1,则
H2O(g) ΔH=+44 kJ·mol-1,则
③此反应用于火箭推进,除释放大量热和快速产生大量气体外还有一个很大的优点是_________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年陕西省西安市远东第一中学高二12月月考化学试卷(带解析) 题型:实验题
⑴有一学生在实验室测某溶液pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
①这种错误操作 (填“一定”/“一定不”/“不一定”)会导致实验结果有误差。
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 。
⑵、用已知浓度的 NaOH 溶液测定某 HCl溶液的浓度,参考右图,从表中选出正确序号 _____________
| 序号 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 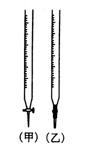 选用滴定管 选用滴定管 |
| A | 碱 | 酸 | 石芯 | (乙) |
| B | 酸 | 碱 | 酚酞 | (甲) |
| C | 碱 | 酸 | 甲基橙 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
| 实验 编号 | 待测氢氧化钠溶液体积(mL) | 滴定开始读数(mL) | 滴定结束读数(mL) | 消耗盐酸体积(mL) |
| ① | 25.00 | 0.02 | 26.40 | |
| ② | 25.00 | 0.04 | 25.81 | |
| ③ | 25.00 | 0.03 | 25.78 | |
| ④ | 25.00 | 0.20 | 25.96 | |
查看答案和解析>>
科目:高中化学 来源:2010年河北省高二上学期期中考试化学试卷 题型:填空题
(1)用标准NaOH溶液滴定未知浓度的盐酸,用酚酞作指示剂,下列操作中会导致实验结果偏低的是 。
①碱式滴定管用蒸馏水洗净后没有用标准液润洗
②用酸式滴定管加待测液时,刚用蒸馏水洗净后的滴定管未用待测液润洗
③锥形瓶用蒸馏水洗净后没有用待测液润洗
④滴定前滴定管尖端有气泡,滴定后气泡消失
⑤终点读数时俯视,其他读数方法正确
(2)有一学生在实验室测某溶液的pH。实验时他先用蒸馏水湿润pH试纸,然后用洁净的玻璃棒蘸取试样进行检测。
①该学生的操作 (填“正确”或“不正确”),如不正确,请分析是否一定有误差并说明理由(若正确则此问不用作答)
。
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 ,原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com