
用密度为 的硫酸溶液,逐滴滴入到
的硫酸溶液,逐滴滴入到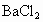 溶液中,直到沉淀恰好完全为止.已知所生成的溶液的质量等于原
溶液中,直到沉淀恰好完全为止.已知所生成的溶液的质量等于原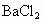 溶液的质量,则
溶液的质量,则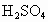 溶液的浓度为
溶液的浓度为
[ ]
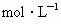
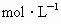
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:013
配制一定物质的量浓度的硫酸溶液(用密度为 的浓硫酸配制
的浓硫酸配制 ),需使用的一组仪器是
),需使用的一组仪器是
[ ]
A.烧杯、托盘天平、量筒、容量瓶、蒸发皿
B.烧杯、量筒、玻璃棒、胶头滴管、容量瓶
C.胶头滴管、烧杯、玻璃棒、容量瓶、分液漏斗
D.量筒、天平、玻璃棒、容量瓶、烧瓶
查看答案和解析>>
科目:高中化学 来源: 题型:021
用密度为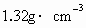 的硫酸溶液,逐滴滴入到
的硫酸溶液,逐滴滴入到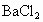 溶液中,直到沉淀恰好完全为止.已知所生成的溶液的质量等于原
溶液中,直到沉淀恰好完全为止.已知所生成的溶液的质量等于原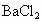 溶液的质量,则
溶液的质量,则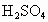 溶液的浓度为
溶液的浓度为
[ ]
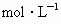
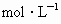
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
配制一定物质的量浓度的硫酸溶液(用密度为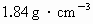 的浓硫酸配制
的浓硫酸配制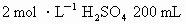 ),需使用的一组仪器是
),需使用的一组仪器是
[ ]
A.烧杯、托盘天平、量筒、容量瓶、蒸发皿
B.烧杯、量筒、玻璃棒、胶头滴管、容量瓶
C.胶头滴管、烧杯、玻璃棒、容量瓶、分液漏斗
D.量筒、天平、玻璃棒、容量瓶、烧瓶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com