
 某同学查阅资料后设计了一条1-丁醇的合成路线:
某同学查阅资料后设计了一条1-丁醇的合成路线:
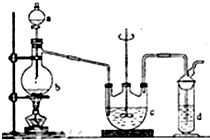
分析 CO的制备方法:HCOOH$→_{△}^{浓硫酸}$CO↑+H2O,在题给装置中,导管a平衡分液漏斗内压强,使分液漏斗内的液体浓硫酸顺利滴下,b主要是起安全瓶的作用,以防止倒吸;c为除去CO中的酸性气体,选用NaOH溶液,还需用d装置除去CO中的H2O,试剂选用浓硫酸;
(1)为了使产生的气体能顺利的从发生装置中排出,就必需保持压强一致,因此a的作用是保持恒压;
(2)用无水硫酸铜检验水,用品红检验二氧化硫,并用酸性高锰酸钾除去二氧化硫,用石灰水检验二氧化碳,最后用酸性高锰酸钾检验乙烯;
(3)题给合成正丁醛的反应为气体体积减小的放热反应,为增大反应速率和提高原料气的转化率;
(4)根据题中物质提纯的流程,粗品中含有正丁醛,利用信息①可知饱和NaHSO3溶液形成沉淀,然后通过过滤即可除去;加入乙醚的目的是萃取溶液中的1-丁醇,1-丁醇和乙醚的沸点相差很大,因此可以利用蒸馏将其分离开.
解答 解:(1)CO的制备方法:HCOOH$→_{△}^{浓硫酸}$CO↑+H2O,反应有气体产生,为了平衡分液漏斗内压强使用导管a,使分液漏斗内的液体浓硫酸顺利滴下,b主要是起安全瓶的作用,防止实验过程中c中液体倒吸入反应装置,
故答案为:导管a平衡分液漏斗内压强,使分液漏斗内的液体顺利滴下.安全瓶b防止实验过程中c中液体倒吸入反应装置;
(2)2-丙醇通过消去反应即到达丙烯,方程式为(CH3)2CHOH$→_{△}^{浓硫酸}$CH2=CHCH3↑+H2O,检验丙烯可以用酸性KMnO4溶液,检验SO2可以用酸性KMnO4溶液褪色、品红溶液或石灰水,检验CO2可以石灰水,检验水蒸气可以无水CuSO4,所以在检验这四种气体必需考虑试剂的选择和顺序.只要通过溶液,就会产生水蒸气,因此先检验水蒸气;然后检验SO2并在检验之后除去SO2,除SO2可以用饱和Na2SO3溶液,最后检验CO2和丙烯,因此顺序为④⑤①②③(或④⑤①③②),
故答案为:④⑤①③②(或④⑤①⑤③②);
(3)由于反应是一个体积减小的可逆反应,所以采用高压,有利于增大反应速率和提高原料气的转化率;正向反应是放热反应,虽然低温有利于提高原料气的转化率,但不利于增大反应速率,因此要采用适当的温度;催化剂不能提高原料气的转化率,但有利于增大反应速率,缩短到达平衡所需要的时间,故正确所选项是D,
故答案为:D;
(4)粗品中含有正丁醛,根据所给的信息利用饱和NaHSO3溶液形成沉淀,然后通过过滤即可除去;由于饱和NaHSO3溶液是过量的,所以加入乙醚的目的是萃取溶液中的1-丁醇;因为1-丁醇和乙醚的沸点相差很大,因此可以利用蒸馏将其分离开,
故答案为:饱和NaHSO3溶液;萃取;蒸馏.
点评 本题考查了气体的制备、有机物的分离、提纯方法、醇的性质以及对基础知识和基本操作的考查,答题时注意把握基础知识和基本实验操作的灵活运用,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原NaOH溶液的浓度是1.00mol/L,所得固体是Na2CO3 | |
| B. | 原NaOH溶液的浓度是0.500mol/L,所得固体是Na2CO3和NaHCO3 | |
| C. | 原NaOH溶液的浓度是1.00mol/L,所得固体是Na2CO3和NaOH | |
| D. | 原NaOH溶液的浓度是0.90mol/L,所得固体是Na2CO3和NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂.它易溶于水,难溶于酒精,受热、遇酸易分解.工业上可用硫化碱法制备,反应原理:
硫代硫酸钠(Na2S2O3)俗名大苏打,可用做分析试剂.它易溶于水,难溶于酒精,受热、遇酸易分解.工业上可用硫化碱法制备,反应原理:| 实验序号 | 1 | 2 | 3 |
| Na2S2O3溶液体积(mL) | 19.98 | 20.02 | 21.18 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 4 种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水用于漂白表现了HClO的强氧化性 | |
| B. | 将一小块金属钠投入稀硫酸铜溶液中会有红色固体析出 | |
| C. | 过氧化钠可用作呼吸面具中的供氧剂 | |
| D. | 等质量的Na2CO3和NaHCO3两种固体,分别与过量盐酸反应,NaHCO3生成CO2的质量比较多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com