
【题目】二十一世纪是钛的世纪。在800~1 000 ℃时电解TiO2可制得钛,装置如图所示。下列叙述正确的是( )

A. a为电源的正极
B. 石墨电极上发生还原反应
C. 阴极发生的反应为TiO2+4e-=Ti+2O2-
D. 每生成0.1 mol钛,转移电子0.2 mol
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】最近科学家发现了一种新分子,它具有空心的类似足球的结构,分子式为C60,下列说法正确的是
A.C60是一种新型的化合物
B.C60和石墨都是碳的同素异形体
C.C60中虽然没有离子键,但固体为离子晶体
D.C60相对分子质量为360
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分类不正确的是( )
A.纯碱、烧碱均属于碱类
B.CO2、SiO2、SO2均属于酸性氧化物
C.醋酸、硫酸、硝酸均属于酸类
D.Na2CO3、Na2SO3、NaCl均属于钠盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2与H2的混合气体加热到850℃时,可建立下列平衡:CO2+H2![]() CO+H2O(g),在一定温度下,平衡时有90% H2变成水,且平衡常数K=1,则原混合气体中CO2与H2的分子数比为( )
CO+H2O(g),在一定温度下,平衡时有90% H2变成水,且平衡常数K=1,则原混合气体中CO2与H2的分子数比为( )
A. 1︰1 B. 1︰5 C. 1︰10 D. 9︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序是( )
①过滤 ②加过量NaOH溶液 ③加适量盐酸
④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
A.①④①②⑤③B.①②④⑤③C.①④②⑤①③D.①②⑤④①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中微粒的物质的量浓度关系正确的是
A. 25 ℃时,向0.1 mol·L-1 NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(NH)>c(SO![]() )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
B. 25 ℃时,NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-7 mol·L-1
C. 0.1![]()
![]() 溶液:
溶液:![]()
D. 相同物质的量浓度的CH3COONa和NaClO的混合液中,各离子浓度的大小关系是:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过碳酸钠(Na2CO3·3H2O2) 在洗涤、纺织、医药等领域有广泛应用。一种制备过碳酸钠的工艺流程如图所示。
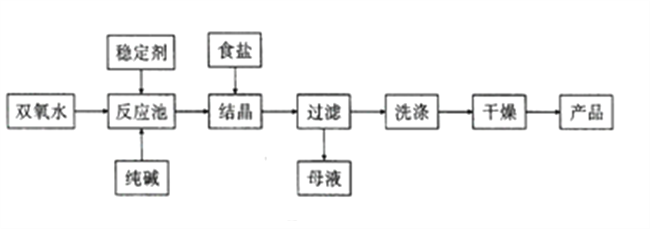
(1)碳酸钠水溶液呈碱性的原因是____________(用离子方程式表示),为增强洗涤效果,可采取最简单的措施是________________。
(2)过碳酸钠受热易分解,写出反应的化学方程式:__________________
(3)稳定剂可能是_____(填序号)。
A.Na2SO3 B.Na2SiO3 C.H2SO4 D.MnO2
(4)结晶时加入食盐的目的是_________,母液中可循环使用的物质是_________(填化学式)。
(5)工业上常以过碳酸钠产品中活性含氧量![]() 来衡量产品优劣,13%以上的为优质品。产品中活性氧含量的测定方法: 称量m g 样品,在250mL 锥形瓶中用100mL 0.5mol/L硫酸完全溶解,立即用c mol/L的高锰酸钾标准溶液进行滴定,至滴定终点,过程中MnO2被还原为Mn2+,进行三次滴定,测得消耗标准溶液平均体积为V1mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗高锰酸钾溶液的体积为V2 mL。该产品活性氧含量为________(用代数式表示)。
来衡量产品优劣,13%以上的为优质品。产品中活性氧含量的测定方法: 称量m g 样品,在250mL 锥形瓶中用100mL 0.5mol/L硫酸完全溶解,立即用c mol/L的高锰酸钾标准溶液进行滴定,至滴定终点,过程中MnO2被还原为Mn2+,进行三次滴定,测得消耗标准溶液平均体积为V1mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗高锰酸钾溶液的体积为V2 mL。该产品活性氧含量为________(用代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com