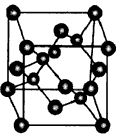
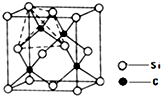
Ⅰ.砷化镓为第三代半导体,以其为材料制造的灯泡寿命长,耗能少。已知砷化镓的晶胞结构如图所示。请回答下列问题:
(1)下列说法正确的是____(填序号)。
A.砷化镓晶胞结构与NaCl相同
B.第一电离能As>Ga
C.电负性As>Ga
D.原子半径As>Ga
(2)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的方程式为_________________;
(3)AsH3空间形状为_______;已知(CH3)3Ga为非极性分子,则其中镓原子的杂化方式为____________;
Ⅱ.金属铜的导电性仅次于银,居金属中的第二位,大量用于电气工业。
(4)请解释金属铜能导电的原因___________,Cu2+的核外电子排布式为_________________
(5)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有___________和____________。

 (2013?青岛一模)[化学-物质结构与性质]
(2013?青岛一模)[化学-物质结构与性质]