
(13分)某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究。
(1)写出甲中反应的化学方程式: 。
(2)乙试管口的棉花应沾有的试剂是 ,其作用是 。
(3)实验小组成员观察乙试管内液体变化是 。
(4)充分反应后,若甲试管中有铜片剩余,继续向甲中加入 溶液,发现铜片溶解,此反应的离子方程式为 。
溶液,发现铜片溶解,此反应的离子方程式为 。
(5)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是 。(填字母)
| A.40.32L | B.30.24L | C.20.16L | D.13.44L |
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案科目:高中化学 来源: 题型:
| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.0 | 3.1 | 8.1 |

查看答案和解析>>
科目:高中化学 来源: 题型:
 实验题:某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究.
实验题:某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
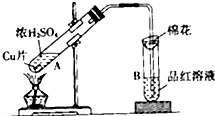 某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究.
某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究.查看答案和解析>>
科目:高中化学 来源: 题型:
草酸(H2C2O4)是一种重要的化工原料。已知常温下0.01 mol·L-l的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示。
|
| H2C2O4 | KHC2O4 | K2C2O4 |
| pH | 2.0 | 3.1 | 8.1 、 |
(1)在其它条件不变时,下列措施能使KHC2O4溶液中c(K+):c(HC2O4-)接近1:1的是_________(填字母)。
A.加入适量的H2C2O4 B.加入适量的KHC2O4
C.加入适量的Na2C2O4 D.升高溶液的温度
(2)取一定质量H2C2O4·2H2O和KHC2O4的混合物,加水溶解,配成250 mL溶液,取两份此溶液各25 mL,向第一份溶液中先加入几滴酚酞试液,再滴加0.25 mol·L-l NaOH溶液至20.00 mL时,溶液由无色变为浅红色;向第二份溶液中滴加适量3 mol·L-l H2S04溶液酸化后,用0.10 mol·L-lKMnO4溶液滴定,当消耗KMnO4溶液16.00 mL时,溶液由无色变为浅紫红色。请回答下列问题:
①完成离子方程式:5C2O42-+2MnO4-+16H+=10______+2Mn2++8H2O。
②原混合物中H2C2O4·2H2O和KHC2O4的物质的量之比为__________。
(3)某实验小组用如图所示的装置探究FeC2O4·2H2O在隔绝空气条件下受热分解的产物。当36.0g FeC2O4·2H2O充分反应后,残留固体质量为13.6g,浓硫酸增重7.2g,碱石灰增重11.0g。求残留固体的成分和物质的量。(已知FeC2O4·2H2O的相对分子质量为180;设反应产生的气体被充分吸收)
查看答案和解析>>
科目:高中化学 来源:2014届吉林省长春市高一上学期期末考试化学试卷 题型:实验题
(13分)某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究。
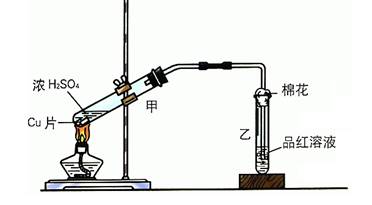
(1)写出甲中反应的化学方程式: 。
(2)乙试管口的棉花应沾有的试剂是 ,其作用是 。
(3)实验小组成员观察乙试管内液体变化是 。
(4)充分反应后,若甲试管中有铜片剩余,继续向甲中加入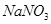 溶液,发现铜片溶解,此反应的离子方程式为
。
溶液,发现铜片溶解,此反应的离子方程式为
。
(5)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是 。(填字母)
A.40.32L B.30.24L C.20.16L D.13.44L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com