
正极材料为![]() 的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
(1)橄榄石型![]() 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过![]() 、
、![]() 与
与![]() 溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
①共沉淀反应投料时,不将![]() 和
和![]() 溶液直接混合的原因是 。
溶液直接混合的原因是 。
②共沉淀反应的化学方程式为 。
③高温成型前,常向![]() 中加入少量活性炭黑,其作用除了可以改善成型后的
中加入少量活性炭黑,其作用除了可以改善成型后的![]() 的导电性能外,还能 。
的导电性能外,还能 。
(2)废旧锂离子电池的正极材料试样(主要含有![]() 及少量AI、Fe等)可通过下列实验方法回收钴、锂。
及少量AI、Fe等)可通过下列实验方法回收钴、锂。

在上述溶解过程中,![]() 被氧化成
被氧化成![]() ,
,![]() 在溶解过程中反应的化学方程式为 。
在溶解过程中反应的化学方程式为 。
![]() 在空气中加热时,固体残留率随温度的变化,如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为 。(填化学式);在350~400℃范围内,剩余固体的成分为 。(填化学式)。
在空气中加热时,固体残留率随温度的变化,如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为 。(填化学式);在350~400℃范围内,剩余固体的成分为 。(填化学式)。

(1)①![]() 在碱性条件下更易被氧化(凡合理答案均可)
在碱性条件下更易被氧化(凡合理答案均可)
②![]()
③与空气中![]() 反应,防止
反应,防止![]() 中的
中的![]() 被氧化
被氧化
(2)①![]() ②
② ![]()
![]() 、
、![]()
本题考察的知识比较散,涉及到能源利用,物质性质、化工流程分析,图表分析,覆盖面比较广。(1)①不能直接混合的原因是Fe2+在碱性条件下更容易被氧化;②根据题给信息,发生的反应为(NH4)2Fe(SO4)2+LiOH+H3PO4=LiFePO4↓+2NH4HSO4+H2O;③消耗空气中的O2,保护Fe2+,防Fe2+被氧化;(2)①通过题给信息可知LiCoO2与Na2S2O3发生了氧化还原反应,反应为8 LiCoO2+ Na2S2O3+11H2SO4=4Li2SO4+8CoSO4+Na2SO4+11H2O。②根据质量的变化,在变化过程中,Co的质量没有变,通过题给数据看,在1000℃是,Co(OH)2完全分解,则产物为CoO;在350~400℃时,固体的质量在89.25%~86.38%之间,可以通过极点进行分析。在290℃时,n(Cr):n(O)=100/93:(89.25-100*59/93)/16=2:3,其化学式为Co2O3,在500℃时n(Cr):n(O)=100/93:(86.38-100*59/93)/16=3:4其化学式为Co3O4,所以可以确定在350~400℃时的化学式为Co3O4和Co2O3。


科目:高中化学 来源: 题型:
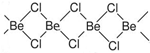 锂和铍单质及化合物的性质具有特殊性.
锂和铍单质及化合物的性质具有特殊性.查看答案和解析>>
科目:高中化学 来源: 题型:022
电池在人们的日常生活、工农业生产、教学、科研等各个方面具有广泛的应 用。电池按不同的划分标准可以划分为不同的种类,用氧化还原反应设计的电池统称 为化学电源。
(1) 化学电源能够把________能转化为________能。组成原电池的条件 之一是________插入电解质溶液中。下列属于化学电源的有_________。①蓄电池 ② 锌锰电池③充电电池④一次性电池
(2)化学电源的组成可以表示为:(一)负极材料‖A‖正极材料(+)。A表示________,
离子在A中的电阻比电子在金属中的电阻________。对于不漏电的电池电子A中 ________(填通过、不通过)。
(3)1991年Sony公司首次推出商品化的锂离子电池,此后锂离子电池,此后锂子电 池的厂家如雨后春笋般在全世界出现,锂离子电池的品种和数量也在逐年增加。锂离 子电池的电压高,单个电池的电压是3.6V。锂离子电池的正极材料是锂的过渡金属氧 化物(例如LiCoO2)混以一定量的导电添加物(例如C)构成的混合导体,负级材料 是可插入锂的碳材料。
①锂在元素周期表中位于第________周期,第________族。②锂离子电池所用的下负 极材料都是不污染环境的无毒无害物质,作为密封电池无毒无害,可以放心使用,属 于绿色能源。而铝镍在生产过程中污染环境。铝镍电池的有毒物质是________,它作 为电池的________级。
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
(1) 化学电源能够把________能转化为________能。组成原电池的条件 之一是________插入电解质溶液中。下列属于化学电源的有_________。①蓄电池 ② 锌锰电池③充电电池④一次性电池
(2)化学电源的组成可以表示为:(一)负极材料‖A‖正极材料(+)。A表示________,
离子在A中的电阻比电子在金属中的电阻________。对于不漏电的电池电子A中 ________(填通过、不通过)。
(3)1991年Sony公司首次推出商品化的锂离子电池,此后锂离子电池,此后锂子电 池的厂家如雨后春笋般在全世界出现,锂离子电池的品种和数量也在逐年增加。锂离 子电池的电压高,单个电池的电压是3.6V。锂离子电池的正极材料是锂的过渡金属氧 化物(例如LiCoO2)混以一定量的导电添加物(例如C)构成的混合导体,负级材料 是可插入锂的碳材料。
①锂在元素周期表中位于第________周期,第________族。②锂离子电池所用的下负 极材料都是不污染环境的无毒无害物质,作为密封电池无毒无害,可以放心使用,属 于绿色能源。而铝镍在生产过程中污染环境。铝镍电池的有毒物质是________,它作 为电池的________级。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:填空题
锂和铍单质及化合物的性质具有特殊性。
I.石墨可以用作锂电池的负极材料,Li+嵌入石墨层间,形成LiC6嵌入式化合物,正极材料常用LixCoO2。
(1)电负性Li Be(填“>”或“<”)。
(2)Co元素基态原子核外价电子排布式为 。
(3)在LiC6中,Li+与相邻石墨六元环的作用力类型为 。
II.固体氯化铍结构如图:
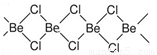
(4)铍原子杂化轨道类型为 。
(5)氯化铍分子中含有化学键类型有 (填序号)。
A.极性键 B.非极性键 C.配位键 D.离子键
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com