
 ,故答案为:
,故答案为: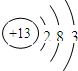 ;
;

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)C、D组成的常见化合物,其水溶液呈碱性,原因是_____________(用离子方程式表示)。写出两种均含A、B、C、D四种元素的化合物相互间发生反应,且生成气体的离子方程式______________________________。
(2)D的单质能跟C的最高价氧化物水化物的浓溶液发生氧化还原反应,生成的两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式_____________。
(3)A、B、D间可形成甲、乙两种微粒,它们均为负一价双原子阴离子且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为_____________。
(4)
(5)用A元素的单质与B元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,两极均有特制的防止透过的隔膜,在A极通入A的单质,B极通入B的单质,则A极是该电池的_______极;B极的电极反应式是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
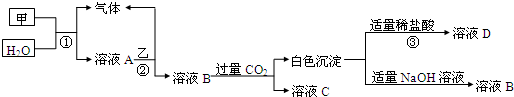
已知甲、乙、丙分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
(1)若甲的化学式为RCl3,其溶液在加热蒸干并灼烧时可发生反应:
a.甲+H2O![]() 乙+丙 b.乙
乙+丙 b.乙![]() 氧化物+H2O
氧化物+H2O
①若甲为某用途广泛的金属元素的氯化物,其溶液在上述变化中生成的氧化物为红
棕色粉末,则该金属在周期表中的位置是 。
②若甲为某短周期金属元素的氯化物,则甲发生a反应的化学方程式为
_ 。
③将以上两种金属单质用导线连接,插入一个盛有NaOH溶液的烧杯中构成原电池,
则负极发生的电极反应为 。
(2)若甲,乙、丙均是短周期中同一周期元素形成的单质或化合物,常温下乙为固体单
质,甲和丙均为气态化合物,且可发生反应:甲+乙![]() 丙。
丙。
则:①甲的结构式为 。
②写出上述反应的化学方程式 。
③写出在200mL 2mol/L的NaOH溶液中通入6.72L(标准状况)的气体甲发生
完全反应的总离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、C是金属单质,A的焰色反应颜色为黄色,B是非金属单质,甲、乙、丙为气体,其中乙是黄绿色气体。(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B 、 C 、丙
(2)乙的水溶液久置过程中发生的反应的化学方程式为:____________________________;_________________________________。
(3)请写出反应①的化学方程式,并用单线桥法标出电子转移的方向和数目:
_________________________________________________。
(4)请写出反应⑤的离子方程式_____________________________________,此反应属于:________________(选填序号)。
a. 化合反应 b. 置换反应
c. 复分解反应 d. 氧化还原反应
(5)写出由物质D、F的水溶液反应生成红褐色沉淀的总的离子方程式:___
_________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com