
| A. | 乙酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O | |
| B. | 甲醛与足量新制Cu(OH)2浊液反应:HCHO+2Cu(OH)2$\stackrel{△}{→}$HCOOH+Cu2O↓+2H2O | |
| C. | 实验室用液溴和苯在催化剂作用下制溴苯: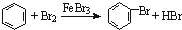 | |
| D. | 将CO2通入苯酚钠溶液: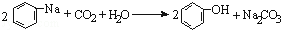 |
分析 A.乙酸为弱酸,离子方程式中乙酸不能拆开;
B.1mol甲醛完全反应生成2mol氧化亚铜,该反应不满足电子守恒;
C.苯与液溴在催化剂存在条件下能够发生取代反应生成溴苯;
D.苯酚的羧酸大于碳酸氢钠,苯酚钠与二氧化碳在溶液中反应生成苯酚和碳酸氢钠.
解答 解:A.CH3COOH为弱酸,在离子方程式中应写成化学式,其正确的离子方程式为:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO-,故A错误;
B.甲醛与足量新制Cu(OH)2浊液反应的离子反应为:HCHO+4Cu(OH)2$\stackrel{△}{→}$H2CO3+2Cu2O↓+4H2O,故B错误;
C.实验室用液溴和苯在催化剂作用下制溴苯的化学反应为: ,故C正确;
,故C正确;
D.碳酸的酸性比苯酚的酸性强,所以苯酚钠通入二氧化碳生成苯酚和碳酸氢钠,正确的化学方程式为:C6H5ONa+CO2+H2O→C6H6OH+NaHCO3,故D错误;
故选C.
点评 本题考查离子反应方程式及化学反应方程式书写的正误判断,为高频考点,题目难度中等,把握发生的反应及离子反应的书写方法为解答的关键,试题侧重有机反应的考查.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子式为C8H10NO2 | |
| B. | 该有机物是苯酚的同系物 | |
| C. | 其属于α-氨基酸的同分异构体有3种 | |
| D. | 该有机物可与FeCl3溶液发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分离出少量氮化硅 | B. | 降低温度 | ||
| C. | 充入氮气 | D. | 充入氦 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
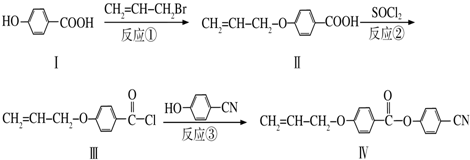
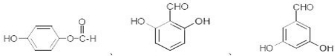 任一种.
任一种.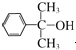 也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是
也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com