
运用有关原理,回答下列问题:(共计10分)
(1)25℃时,某FeCl3溶液的pH=2,则此溶液中由水电离产生的c(H+)= ,用离子方程式表示CH3COONa溶液呈碱性的原因: 。
(2)已知NaHSO4在水中的电离方程式为NaHSO4===H+ + SO42-+ Na+。在NaHSO4溶液中,c(H+) c(OH-)+ c(SO42-)(填“﹤”“﹥”或“=”,下同);室温下用NaHSO4溶液与Ba(OH)2溶液制取BaSO4,若溶液中的SO42-完全沉淀,则反应后溶液的pH 7。
(3)已知Ksp(BaSO4)=1.1×10-10。将等体积的Na2SO4溶液和BaCl2溶液混合,若Na2SO4溶液的浓度为0.02mol/L,则生成BaSO4沉淀所需的BaCl2溶液的最小浓度为 。
(忽略溶液混合时体积的变化)
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法不正确的是
①将BaSO4放入水中不能导电,所以BaSO4是非电解质
②氨溶于水得到的氨水能导电,所以氨水是电解质
③固态共价化合物不导电,熔融态的共价化合物可以导电
④固态的离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
A.①④ B.①④⑤ C.①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三第一次月考试卷化学试卷(解析版) 题型:选择题
(10分)有一混合物的水溶液,只可能含以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32-、SO42 -,现取三份100 mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生。
②第二份加过量NaOH溶液加热后收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。
③在甲溶液中通过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g。
④第三份加足量BaCl2溶液后得白色沉淀,沉淀经足量盐酸洗涤干燥后质量为11.65 g。
根据上述实验回答: ___________, 不能确定是否存在的离子是________________。
(2)试确定溶液中肯定存在的阴离子及其浓度(可不填满):
离子符号______,浓度_____________;
离子符号______,浓度_______________;
离子符号______,浓度________________;
(3)试确定K+ 是否存在________(填“是”或“否”),判断的理由是 ______________。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三上学期一模化学试卷(解析版) 题型:选择题
下表各组物质中,物质之间不可能实现如图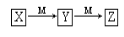 所示转化的是
所示转化的是
选项 | X | Y | Z | M |
A | Fe(s) | FeCl2 | FeCl3 | Cl2 |
B | NaOH(aq) | Na2CO3 | NaHCO3 | CO2 |
C | NH3(g) | NO | NO2 | O2 |
D | S(s) | SO2 | SO3 | O2 |
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列离子方程式不正确的是
A.向Na2FeO4溶液中加入稀硫酸产生氧气:4FeO42—+20H+ = 4Fe3++3O2↑+10H2O
B.10mL0.5mol/L的明矾溶液与20mL0.5mol/LBa(OH)2溶液混合反应:3Ba2+ + 6OH- +2Al3+ +3SO42- = 3BaSO4↓+2Al(OH)3↓
C.铜粉与63%的硝酸反应:Cu +4H++2NO3- =Cu2++2NO2↑+ 2H2O
D.工业上用纯碱液吸收SO2:CO32-+SO2=CO2+SO32-
查看答案和解析>>
科目:高中化学 来源:2016届贵州省遵义市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列各组单质中,前者能将后者从化合物中置换出来的是
①Al Fe ②C Si ③Cu H2 ④H2 Cu
A.只有①② B.只有②④ C.只有①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上化学试卷(解析版) 题型:填空题
(12分)现有A、B、C、D、E、F六种短周期元素,原子序数依次增大。已知A与D、C与E分别同主族,D、E、F同周期。A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C可形成电子总数相等的分子,且A与C、A与E、A与F也可以形成电子总数相等的分子。
请回答下列问题:
(1)元素F在周期表中的位置___________。
(2)A、C、D三种元素可组成一种常见化合物,该化合物的化学式为_______ _;
该化合物和单质F反应的离子方程式为_______________。
(3)B与F形成的化合物分子中,各原子最外层均达8电子结构,则该分子的电子式为_____ ___。
(4)已知0.50 mol EC2被C2氧化成气态EC3,放出49.15 kJ热量,其热化学方程式为____________。
(5)A、B、C以原子个数比4∶2∶3所形成的化合物,所含的化学键类型为 __。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江大庆铁人中学高二上9月考化学试卷(解析版) 题型:选择题
决定化学反应速率快慢的因素是
A、温度 B、浓度 C、催化剂 D、反应物的性质
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期一模化学试卷(解析版) 题型:选择题
下列反应中,改变反应物的用量或浓度,不会改变生成物的是
A.铜和硝酸反应 B.二氧化碳通入氢氧化钠溶液中
C.细铁丝在氯气中燃烧 D.氯化铝与氢氧化钠溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com