
(2)AlCl3与NaOH溶液反应,当Al3+与OH-的物质的量之比为________时沉淀最多,________时沉淀全部溶解,________时沉淀为最多时的一半。
(3)现代科学实验证明,溶液中不存在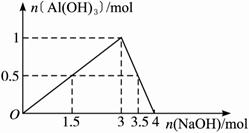 ,应为[Al(OH)-4],
,应为[Al(OH)-4], 是沿用旧的书写习惯。请写出Al2(SO4)3溶液与过量NaOH溶液反应的化学方程式(不能用偏铝酸盐表示):______________________。
是沿用旧的书写习惯。请写出Al2(SO4)3溶液与过量NaOH溶液反应的化学方程式(不能用偏铝酸盐表示):______________________。
解析:(2)(图象法):由下列反应得到下图:

Al3++3OH-══Al(OH)3↓
Al3++4OH-══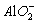 +2H2O
+2H2O
设n(AlCl3)=1 mol,可见:Al3+与OH-的物质的量之比为1∶1.5或1∶3.5时,沉淀为最大量的一半。
(3)写成偏铝酸盐的形式
Al2(SO4)3+8NaOH══2NaAlO2+3Na2SO4+4H2O
并把Al(OH)-4看作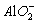 ·2H2O,将Al(OH)
·2H2O,将Al(OH)![]() 取而代之可得答案。
取而代之可得答案。
答案:(1)氨水是弱碱,NaOH是强碱,过量的氨水不能溶解Al(OH)3,而过量的NaOH能溶解Al(OH)3。故实验室中制取Al(OH)3用氨水而不用NaOH
(2)1∶3 1∶4 2∶3或2∶7
(3)Al2(SO4)3+8NaOH══2Na[Al(OH)4]+3Na2SO4


科目:高中化学 来源: 题型:038
往V L Al2(SO4)3溶液中通入过量NH3,使Al(OH)3沉淀下来,滤出沉淀,经灼烧、电解然后与适量的铁红混合加热.再将加热后的产物用NaOH溶液处理,最后得m g固体,求原溶液中SO![]() 的物质的量的浓度为 (
)
的物质的量的浓度为 (
)
A.![]() mol·L-1
mol·L-1
B.![]() mol·L-1
mol·L-1
C.![]() mol·L-1
mol·L-1
D.![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:038
A.![]() mol·L-1
mol·L-1
B.![]() mol·L-1
mol·L-1
C.![]() mol·L-1
mol·L-1
D.![]() mol·L-1
mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com