
(10分)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中的溶质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为________(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为_____________。
(2)丙池中F电极为________(填“正极”、“负极”、“阴极”或“阳极”),该池总反应的化学方程式为____________________________________________________________。
(3)当乙池中C极质量减轻4.32 g时,甲池中B电极理论上消耗O2的体积为________mL(标准状况)。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是________(填字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
(1)原电池(1分) CH3OH+8OH--6e-===CO32-+6H2O(2分)(2)阴极(1分) 2CuSO4+2H2O===2H2SO4+2Cu+O2↑(2分)(3)224mL(2分)(4)A(2分)
【解析】
试题分析:(1)从图可以看出甲是一个甲醇燃料电池,燃料电池是原电池,在燃料电池中燃料反应的一极是负极,氧气反应的一极是正极,所以A是负极、B是正极,由于电解质溶液是KOH溶液,所以甲醇反应生成的CO2不能以气体的形式释放出去,而是与OH-反应生成CO32-,则A电极反应方程式为:2CH3OH+16OH--12e-===2 CO32-+12H2O。(2)甲是原电池,那么乙和丙都是池为电解池,丙中F接原电池的负极,作阴极,丙池中就是用惰性材料电解CuSO4溶液,电池的总反应为:2CuSO4+2H2O===2H2SO4+2Cu+O2↑。(3)乙池中C接电源的正极,作为阳极,Ag是活性材料,所以是Ag放电,电极反应为:Ag- e-=Ag+,C极质量减轻4.32g,则反应的Ag的物质的量为:4.32g÷108g/mol=0.04mol,根据反应知道反应0.04molAg时转移的电子为0.04mol,再根据B电极反应式为:O2+4e-+ 2H2O=4OH-,转移0.04mol电子时反应的O2的物质的量为0.01mol,O2体积为0.01 mol×22.4L/mol=0.224L=224mL。(4)电解时乙池中C的电极反应为:Ag- e-=Ag+,D的电极反应为Cu2++2e-=Cu,可以看出溶液中多了Ag+,少了Cu2+,要恢复反应前的浓度可以加入Cu,将其中的Ag+置换出来即可,选A。
考点:原电池和电解池的判断、原电池和电解池的工作原理、电极反应的书写、电子转移的计算等。


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源:2014-2015学年甘肃省兰州市高三下学期诊断考试理综化学试卷(解析版) 题型:填空题
[化学—选修3:物质结构与性质](15分)
在周期表中1~36号之间的A、B、C、D、E、F六种元素,它们的原子序数依次增大,已知A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C元素原子的最外层有3个自旋方向相同的未成对电子,D原子核外电子有8种不同的运动状态,E元素在第四周期,E的基态原子中未成对电子数是核外电子总数的1/4,F元素位于周期表的ds区,其基态原子最外能层只有一个电子。
(1)写出基态E原子的价电子排布式 。
(2)B、C、D三种元素第一电离能由小到大的顺序为 (用元素符号表示)。
(3)A与C形成CA3型分子,分子中C原子的杂化类型为 ,分子的立体结构为 ;C的单质与化合物BD是等电子体,根据等电子体原理,写出化合物BD的电子式 。
(4)A2D的沸点在同族元素中最高,其原因是 。A2D由液态形成晶体时密度 (填“增大”、“不变”或“减小”),其主要原因 (用文字叙述)。
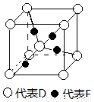
(5)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为 (用元素符号表示);若相邻D原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为 g·cm-3(用含a、NA的符号表示)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省龙岩市高三教学质量检查理综化学试卷 (解析版) 题型:选择题
已知:NH2COO-+2H2O  HCO3-+NH3·H2O。现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示。以下分析正确的是
HCO3-+NH3·H2O。现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示。以下分析正确的是

A.无法判断T1和T2的大小关系
B.T1 ℃时,第6min反应物转化率为6.25%
C.T2 ℃时,0~6min ν(NH2COO-)=0.3mol·L-1·min-1
D.往平衡体系加水稀释,平衡右移,溶液中各种离子浓度减小
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省深圳市南山区上学期高一化学期末试卷(解析版) 题型:选择题
根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是
①I2 + SO2 + 2H2O = H2SO4 + 2HI
②2FeCl2 + Cl2 = 2FeCl3
③2FeCl3 + 2HI = 2FeCl2 + 2HCl+I2
A.SO2>I->Fe2+>Cl- B.Cl->Fe2+>SO2>I-
C.Fe2+>I->Cl->SO2 D.I->Fe2+>Cl->SO2
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省深圳市南山区上学期高一化学期末试卷(解析版) 题型:选择题
下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是
①金属钠在纯氧中燃烧 ②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间
③FeCl3溶液中滴入KSCN溶液 ④无水硫酸铜放入医用酒精中
A.②③①④ B.③②①④ C.③①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市等三校高二上学期期末化学试卷(解析版) 题型:选择题
下列水解的离子方程式正确的是
A.S2﹣+2H2O H2S+2OH﹣ B.Fe3++3H2O
H2S+2OH﹣ B.Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
C.HCO3﹣+H2O CO32﹣+H3O+ D.HS﹣+H2O
CO32﹣+H3O+ D.HS﹣+H2O H2S ↑ + OH﹣
H2S ↑ + OH﹣
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省汕头市等三校高二上学期期末化学试卷(解析版) 题型:选择题
下列有关金属腐蚀与防护的说法正确的是
A.银器表面在空气中因电化腐蚀渐渐变暗
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省揭阳市高二上学期期末考试化学文试卷(解析版) 题型:?????
下列实验现象描述正确的是
A.氯化氢与氨气相遇,有大量的白雾生成
B.用铂丝蘸取硫酸钠溶液,灼烧火焰呈黄色
C.氯化亚铁溶液与无色的KSCN溶液混合,溶液呈红色
D.SO2通入品红溶液,红色褪去,再加热,红色不再重现
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com