
分析 (1)沙子不溶于水,食盐溶于水;KNO3和NaCl的溶解度受温度影响不同;
(2)③中水和汽油分层;
(3)蒸发、蒸馏实验中均需要酒精灯.
解答 解:(1)沙子不溶于水,食盐溶于水,则分离①的操作是过滤;KNO3和NaCl的溶解度受温度影响不同,则分离②的操作是结晶,
故答案为:过滤;结晶;
(2)③中水和汽油分层,则需要的仪器为分液漏斗,在其它组分离时无需使用,故答案为:分液漏斗;
(3)蒸发、蒸馏实验中均需要酒精灯,则上述四组分离时需使用酒精灯的有②、④,故答案为:②;④.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意仪器的使用,题目难度不大.


科目:高中化学 来源: 题型:实验题
 可逆反应Fe(s)+CO2(g)?FeO(s)+CO(g),在温度938K时,平衡常数K=1.47,在1173K时,K=2.15.
可逆反应Fe(s)+CO2(g)?FeO(s)+CO(g),在温度938K时,平衡常数K=1.47,在1173K时,K=2.15.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 描述 | 解释 |
| A | 凡火药,硫为纯阳,硝为纯阴,此乾坤幻出神物也 | “硝”指的是硝酸钾 |
| B | 凡墨烧烟凝质而为之 | “烟”指的是焦炭 |
| C | 凡墨伪方士以炉火惑人者,唯朱砂银愚人易惑 | “朱砂银”指的是Ag2S |
| D | 五金之长,熔化成形之后,住世永无变更 | 这名话描述的对象为Cu |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类在一定条件下都可以水解生成乙醇和二氧化碳 | |
| B. | 乙酸乙酯和油脂都属于酯类物质,碱性条件水解称之为皂化反应 | |
| C. | 硝酸汞溶液加入到鸡蛋清中,可以使蛋清液盐析而沉淀下来 | |
| D. | 淀粉在稀硫酸加热催化下,水解产物葡萄糖的检出,先加入NaOH溶液后加入银氨溶液水浴加热,看是否有银镜出现.若出现银镜,证明有葡糖糖生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
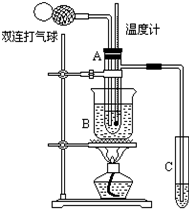 乙醛(CH3CHO)在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次,反应基本完全.有关物质的沸点见表:
乙醛(CH3CHO)在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次,反应基本完全.有关物质的沸点见表:| 物质 | 乙醛 | 乙酸 | 甘油 | 乙醇 | 水 |
| 沸点/℃ | 20.8 | 117.9 | 290 | 78.2 | 100 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com