
水溶液中能大量共存的一组离子是
A、NH4+、Ba2+、Br-、CO32-
B、Cl-、MnO4-、Fe2+、K+
C、K+、Na+、SO42-、MnO4-
D、Na+、H+、NO3-、HCO3-
科目:高中化学 来源:2016届山东师大附中高三上学期第二次模拟考试化学试卷(解析版) 题型:选择题
下列叙述中正确的是( )
A.SiO2和NO2能与强碱溶液反应,都是酸性氧化物
B.不锈钢材料因含有铬、镍所以抗腐蚀性好
C.普通玻璃、钢化玻璃、玻璃钢都属于硅酸盐产品,水玻璃可用于木材防腐
D.MgO和A12O3熔点较高都可以做耐火材料,都能和强碱溶液反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州十校联合体高二上学期期中测试化学试卷(解析版) 题型:选择题
已知反应①:CO(g)+CuO(s) 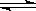 CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②:H2(g)+CuO(s) 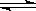 Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g) 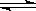 CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是
A.反应①的平衡常数K1=
B.反应③的平衡常数K=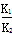
C.对于反应③,恒容时,温度升高,H2浓度减小,则该反应的△H>0
D.对于反应③,恒温恒容下,增大压强,H2浓度一定减小
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期期中联考化学试卷(解析版) 题型:选择题
下列溶液中的离子一定能大量共存的是
A.在加入铝粉能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3-
B.室温下由水电离出的氢离子浓度c(H+)=1×10-14mol/L的溶液中:Ba2+、NO3-、K+、ClO-
C.能使酚酞变红色的溶液中:Na+、K+、AlO2-、CO32-
D.含大量Fe3+的溶液中:NH4+、Na+、C1-、SCN-
查看答案和解析>>
科目:高中化学 来源:2016届湖南省澧县、桃源、益阳三校高三上学期联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.非金属不可能形成阳离子
B.两种酸溶液混合不可能呈中性
C.中和反应一定是放热反应
D.金属不可能形成阴离子
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川市高三上学期统练(三)化学试卷(解析版) 题型:选择题
利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。下列说法不正确的是

A.电流从右侧电极经过负载后流向左侧电极
B.A电极上发生氧化反应,B为正极
C.电极A极反应式为2NH3-6e-=N2+6H+
D.当有2.24LNO2(标准状况)被处理时,转移电子为0.4mol
查看答案和解析>>
科目:高中化学 来源:2016届辽宁师范大学附属中学高三上学期期中考试化学试卷(解析版) 题型:选择题
下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中 ②过量Ba(OH)2浓溶液和AlNH4(SO4)2溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中 ⑤Na2S2O3溶液中加入稀硫酸
A.只有①②④⑤ B.只有③ C.只有②③ D.只有①④⑤
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期期中考试化学试卷(解析版) 题型:选择题
能大量共存于同一溶液中,且当加入另一种强电解质使水电离出的c(H+) = 1×10-13 mol·L-1 时,又一定能发生反应的离子组是( )
①Fe3+ 、NH4+ 、SCN-、Cl- ②K+ 、Na+ 、Cl- 、HCO3- ③Fe2+ 、Na+ 、NO3-、Br-
④Al3+ 、Na+ 、HCO3- 、NO3- ⑤K+ 、NH4+ 、CH3COO-、SO42- ⑥Na+ 、K+ 、CH3COO- 、NO3-
A.④⑤⑥ B.①④⑤ C.②④⑥ D.②③⑤
查看答案和解析>>
科目:高中化学 来源:2016届浙江宁波效实中学高三上学期期中考试化学试卷(解析版) 题型:选择题
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。下列分析正确的是
A.上述实验条件下,物质的氧化性:Cu2+ > I2 > SO2
B.通入SO2时,SO2与I2反应,I2作还原剂
C.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性
D.滴加KI溶液时,转移2 mol e- 时生成1 mol白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com