
| A、+2a | ||
| B、+a | ||
C、+
| ||
D、+
|
| a |
| 2 |


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
| A、加热硫酸、乙醇、氯化钠固体的混合物制氯乙烷 |
| B、福尔马林与苯酚的混合物,沸水浴加热制酚醛树脂 |
| C、氯乙烯加聚的生成物能使酸性KMnO4溶液褪色 |
| D、苯与浓溴水反应(Fe作催化剂)制溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba2+、Cl-、SO42-、K+ |
| B、Mg2+、SO42-、Na+、Cl- |
| C、H+、CO32-、Al3+、Cl- |
| D、K+、Fe2+、NO3-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用过滤法除去Fe(OH)3胶体中的FeCl3 |
| B、为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 |
| C、向某溶液中滴入BaCl2溶液和稀HNO3,来检验溶液中是否含有SO42- |
| D、将Na投入到CuSO4溶液中置换出铜,来证明钠的金属性比铜强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
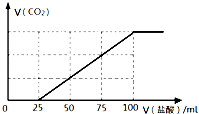 向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )
向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )| A、原NaOH溶液的浓度为0.2 mol/L |
| B、通入CO2的体积为448 mL |
| C、所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3)=1:3 |
| D、所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3)=1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡能发生银镜反应的有机物一定是醛 |
| B、酸和醇发生的反应一定是酯化反应 |
| C、乙醇易溶于水是因为分子间形成了一种叫氢键的化学键 |
| D、在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢而生成水和酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/浓度 | c(NH3)(mol?L-1) | c(O2)(mol?L-1) | c(NO)(mol?L-1) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.7 | 1.475 | 0.1 |
| 第10min | 0.7 | 1.475 | 0.1 |
| A、反应在第2min到第4min时,O2的平均速率为0.1875mol?L-1?min-1 |
| B、反应在第2min时改变了某一条件,该条件可能是使用催化剂或升高温度 |
| C、第4min、第8min时分别达到化学平衡,且平衡常数相同 |
| D、在开始反应的前2min内,该反应放出0.05QKJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com