
【题目】下列离子方程式书写正确的是( )
A.铁投入硫酸锌溶液中:Fe+Zn2+═Zn+Fe2+
B.钠投入硫酸铜溶液中:2Na+Cu2+═Cu+2Na+
C.往饱和Na2CO3溶液中逐滴加入少量稀盐酸: ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
D.钠投入冷水中:2Na+2H2O═2Na++2OH﹣+H2↑
科目:高中化学 来源: 题型:
【题目】工业上利用H2SiF6溶液制备BaF2 , 同时可得到副产品SiO2 , 其工艺如下:
已知:焙烧过程的反应为(NH4)2SiF6+BaCO3 ![]() BaSiF6+2NH3↑+CO2↑+H2O↑
BaSiF6+2NH3↑+CO2↑+H2O↑
(1)焙烧的气体产物能恰好完全反应生成物质A,则A的化学式为 .
(2)氨解反应为放热反应,且反应能进行完全.该反应需降温冷却的原因为、 .
(3)热解的另一产物是含两种元素的气体,该气体水解的化学方程式是 .
(4)SiO2可用于制作 , 该物质在信息传输中具有重要应用.
(5)为保持该过程的持续循环,每生成1mol BaF2 , 理论上需补充原料H2SiF6mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质和用途的说法,错误的是
A.硅酸钠可作建筑行业的黏合剂
B.Na-K合金可作为快中子反应堆的导热剂
C.晶体硅是在通信工程中制作光导纤维的主要原料
D.氧化铁常用于红色油漆和涂料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】圣路易斯大学研制的新型乙醇燃料电池,用能传递质子(H+)的介质作溶剂,反应为C2H5OH+3O2→2CO2+3H2O,如图是该电池的示意图,下列说法正确的是( ) 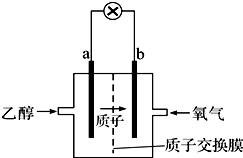
A.a极为电池的正极
B.电池正极的电极反应为:4H++O2+4e﹣═2H2O
C.电池工作时电流由a极沿导线经灯泡再到b极
D.电池工作时,1mol乙醇被氧化时就有6 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种烃.已知①1mol五种烃分别完全燃烧,都生成134.4L CO2(标准状况);且烃C完全燃烧时,生成的水的物质的量比CO2多;
②A和D都能使溴水褪色,其中1mol D可以和1mol H2反应生成1mol A;1molA又可继续和1mol H2反应又生成1mol C;
③C不与溴水或酸性KMnO4溶液反应;
④A存在多种同分异构体,其中C只能由一种A与氢气反应而得;
⑤B在铁屑存在下可以跟液溴反应,但不与溴水或酸性高锰酸钾溶液反应;
⑥B能和氢气充分反应生成E;
请回答下列问题:
(1)写出所属烃的类别:A , B , C .
(2)烃C的一卤代产物有种同分异构体.
(3)用“系统命名法”对D命名: .
(4)以上几种物质能作为溴水中溴的萃取剂的有:(用“A,B,C…”作答).
(5)写出符合题设条件的A与HCl在催化剂作用下的加成反应方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1molH2O的质量是18g/mol B. CH4的摩尔质量为16g
C. 3.01×1023个SO2分子质量为32g D. 2molNaOH溶于1L水中配成溶液的浓度为2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】勒夏特列原理适用于许多平衡体系。试用该原理分析水的电离平衡(H2O![]() H++OH-),填写下列表格(除④外,其余都假设溶液温度不变):
H++OH-),填写下列表格(除④外,其余都假设溶液温度不变):
改变条件 | 平衡移动方向 | c(H+)的变化 | c(OH-)的变化 | Kw |
①加入醋酸 | ||||
②加入烧碱 | ||||
③加入CH3COONa | ||||
④升高温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com