
【题目】铁是生产生活中应用最广泛的一种金属。某化学学习小组在实验室中探究铁钉(主要成分为低碳钢)与热浓硫酸的反应。其探究流程如图所示:
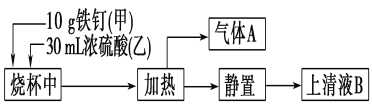
(1)从实验安全的角度考虑,应先向烧杯中加入______(填“甲”或“乙”);根据加入的反应物的量,实验需要选取的烧杯的规格为________(填字母序号)。
a.50 mL b.100 mL c.500 mL d.1 000 mL
(2)上清液B中可能既含Fe3+,又含Fe2+,要检验上清液B中有无Fe2+,应加入的试剂是________(填字母序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.NaOH溶液 d.酸性KMnO4溶液
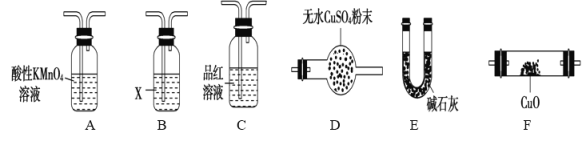
(3)气体A的主要成分是SO2,还可能含有H2和CO2。流程图中“加热”时可能生成CO2的原因是(用化学方程式表示)___________________。利用下列仪器可以同时检验气体A中是否含有H2和CO2(其中的夹持仪器、橡胶管和加热装置已经略去),则仪器的连接顺序是____________
(4)烧杯中的产物之一FeSO4有如下转化关系 (无关物质已略去)。
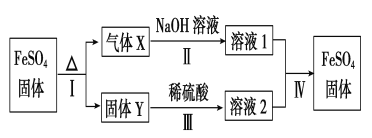
已知:①X由两种化合物组成,将X通入品红溶液,溶液褪色;通入BaCl2溶液,产生白色沉淀。②Y是红棕色的化合物。反应Ⅰ的化学方程式为_________________X通入BaCl2溶液,产生白色沉淀的化学式为________
【答案】甲 b d C+2H2SO4(浓)![]() 2SO2↑+CO2↑+2H2O ACBEFDE 2FeSO4
2SO2↑+CO2↑+2H2O ACBEFDE 2FeSO4 ![]() Fe2O3+SO2↑+SO3↑ BaSO4
Fe2O3+SO2↑+SO3↑ BaSO4
【解析】
(1)先在烧杯中加铁钉,再加浓硫酸;烧杯中所盛反应的液体不能超过容积的一半;
(2)Fe2+具有还原性,能使酸性KMnO4溶液褪色;
(3)铁钉中含有少量的碳元素,C与浓硫酸反应生成二氧化碳、二氧化硫和水;
检验气体A中是否含有H2和CO2,应该先除去二氧化硫,然后用澄清石灰水检验二氧化碳,再干燥,然后通过CuO,与CuO反应生成水,用无水硫酸铜检验水的生成,即可证明有氢气.
(4)FeSO4分解得到气体X与红棕色固体Y,X由两种化合物组成,将X通入品红溶液,溶液褪色,而X通入BaCl2溶液,产生白色沉淀,则X为SO2、SO3混合物,结合转化关系可知Y为Fe2O3;
反应Ⅰ的反应方程式为:2FeSO4 ![]() Fe2O3+SO2↑+SO3↑;
Fe2O3+SO2↑+SO3↑;
X为SO2、SO3混合物,溶于水生成物中含有硫酸,与BaCl2溶液,产生白色沉淀为BaSO4。
(1)先在烧杯中加铁钉,再加浓硫酸,如果先加入浓硫酸,再加铁钉,则容易溅起浓硫酸伤人;根据加入的反应物的量,实验需要选取的烧杯的规格要大于30ml×2,故选100ml,即选b。
(2)由于铁钉生锈,上清液B中可能既含Fe3+,又含Fe2+,Fe2+具有还原性,能使酸性KMnO4溶液褪色,所以用酸性KMnO4溶液检验有无Fe2+;
故答案为:d;
铁钉中含有少量的碳元素,C与浓硫酸反应生成二氧化碳、二氧化硫和水,其反应的方程式为:C+2H2SO4(浓)![]() 2SO2↑+CO2↑+2H2O;
2SO2↑+CO2↑+2H2O;
检验气体A中是否含有H2和CO2,应该先除去二氧化硫,所以把混合气体通过酸性KMnO4溶液,再通过酚酞试液检验二氧化硫是否吸收完全,然后把气体通过澄清石灰水,用澄清石灰水检验二氧化碳,再通过碱石灰干燥,然后通过灼热CuO,氢气与CuO反应生成水,用无水硫酸铜检验水的生成,即可证明有氢气,所以仪器的连接顺序是ACBEFDE;
(4)FeSO4分解得到气体X与红棕色固体Y,X由两种化合物组成,将X通入品红溶液,溶液褪色,而X通入BaCl2溶液,产生白色沉淀,则X为SO2、SO3混合物,结合转化关系可知Y为Fe2O3。
反应Ⅰ的反应方程式为:2FeSO4 ![]() Fe2O3+SO2↑+SO3↑;
Fe2O3+SO2↑+SO3↑;
X为SO2、SO3混合物,溶于水生成物中含有硫酸,与BaCl2溶液,产生白色沉淀为BaSO4。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案科目:高中化学 来源: 题型:
【题目】将固体NH4Br置于密闭容器中,在某一温度下,发生下列反应:NH4Br![]() NH3(g) + HBr(g) ; 2HBr
NH3(g) + HBr(g) ; 2HBr![]() H2(g) + Br2(g) ,两分钟后测知H2为0.5mol/L ,HBr为4mol/L ,若NH4Br 的分解速率用v(NH3)表示,下列速率正确的是( )
H2(g) + Br2(g) ,两分钟后测知H2为0.5mol/L ,HBr为4mol/L ,若NH4Br 的分解速率用v(NH3)表示,下列速率正确的是( )
A. 0.5mol·L-1·min-1 B. 2.5 mol·L-1·min-1
C. 2mol·L-1·min-1 D. 1.2 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盆烯的分子结构如图所示(其中碳、氢原子均已略去)。关于盆烯的说法正确的是

A. 盆烯的一氯取代物有3种
B. 盆烯是乙烯的一种同系物
C. 盆烯是苯的一种同分异构体
D. 盆烯为不饱和烃,能与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 mol某烃在足量的氧气中完全燃烧,生成水和二氧化碳各6 mol,则该烃的分子式为________ ;若该烃能使溴水褪色,在催化剂作用下,与H2发生加成反应,生成2,2-二甲基丁烷,则该烃的结构简式为 ________________________;写出该烃在催化剂作用下发生加聚反应的化学方程式: ______________。;若该烃不能使溴水褪色,但一定条件下能跟溴发生取代反应,其一溴取代物只有一种,则该烃的结构简式为________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的正确组合是( )
类别 组合 | 酸性氧化物 | 碱性氧化物 | 酸 | 碱 | 盐 |
A | CO2 | SiO2 | H2SO4 | Na2CO3 | NaHCO3 |
B | CO | Na2O | HCl | NaOH | NaCl |
C | SO2 | CuO | CH3COOH | KOH | CaF2 |
D | SO3 | CaO | HNO3 | Ca(OH)2 | CaCO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语描述中不正确的是( )
A. 中子数为20的氯原子:![]()
B. K2O的电子式:![]()
C. HCO3﹣的电离方程式:HCO3﹣+H2O![]() CO32﹣+H3O+
CO32﹣+H3O+
D. 比例模型![]() 可以表示CO2分子或SiO2
可以表示CO2分子或SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取镁的工艺流程可表示如下:
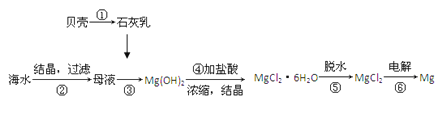
下列说法不正确的是
A. 用此法提取镁的优点之一是原料来源丰富
B. 步骤⑥电解熔融MgCl2时可制得Mg(OH)2
C. 步骤⑤可将晶体置于HCl气体氛围中脱水
D. 上述工艺流程中涉及化合、分解和复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 盐酸和氨水反应H++OH=H2O、B. 钠和冷水反应Na+2H2O=Na++2OH+H2↑
C. 氯气和氢氧化钠溶液反应Cl2+2OH=Cl+ClO+H2OD. 铜和稀硝酸反应Cu+2NO3+4H+=2Cu2++2NO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是 ( )

A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C. 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
D. 图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com