
在100g碳不完全燃烧所得气体中,CO占1/3,CO2占2/3,且
C(s)+1/2O2(g)=CO(g) △H=-110.35kJ/mol;
CO(g)+1/2O2(g)=CO2(g);△H=-282.57 kJ/mol,
与这些碳完全燃烧相比,损失的热量是
A.392.92kJ B.2489.44kJ
C.3274.3kJ D.784.92kJ
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源:2016届贵州省高三上学期第二次月考理综化学试卷(解析版) 题型:填空题
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为________________;A、B、C的电负性由大到小的顺序为___________;(均用“<”或“>”连接)
(2)B的氢化物的分子空间构型是_____________。其中心原子采取_____________杂化。
(3)写出化合物AC2的电子式____________;一种由B、C组成的化合物与AC2互为等电子体,其化学式为____________。
(4)E的价层电子排布式是____________,在形成化合物时它的最高化合价为_____________,ECl3形成的配合物的化学式为________________。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是________________。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
S2Cl2在合成橡胶、硬水软化等方面有着重要应用。将Cl2通入熔融的硫磺可制得S2Cl2,S2Cl2是黄红色油状发烟液体,遇水分解出无色有刺激性气味的气体,且溶液变浑浊。有关叙述正确的是
A.在周期表中,氯元素位于硫元素之后,所以Cl2的氧化性弱于硫单质
B.Cl2与硫磺的反应中,S2Cl2只是氧化产物
C.在常温常压下,硫磺是原子晶体,S2Cl2是分子晶体
D.S2Cl2与水反应时,既体现氧化性又体现还原性
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古巴彦淖尔高一上10月月考化学试卷(解析版) 题型:选择题
实验室中需要配制1mol/L的NaCl溶液970mL,配制时应选用的容量瓶的规格是
A.950mL 容量瓶 B.500mL容量瓶
C.1000mL 容量瓶 D.任意规格的容量瓶
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
在温度不变的条件下,在恒容的容器中进行下列反应:N2O4(g)=2NO2(g),若N2O4的浓度由0.1mol•L-1降到0.07mol•L-1需要15s,那么N2O4的浓度由0.07mol•L-1降到0.05mol•L-1所需的反应时间
A.等于5s B.等于10s C.大于10s D.小于10s
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上学期9月月考化学试卷(解析版) 题型:选择题
在25℃、1.01×105Pa时,1gCH4燃烧时生成CO2与液态H2O,放出55.6kJ的热量,则CH4的燃烧热为
A.55.6kJ/mol B.889.6kJ/mol C.-889.6kJ/mol D.444.8kJ/mol
查看答案和解析>>
科目:高中化学 来源:2016届福建省莆田市高三上学期第一次月考化学试卷(解析版) 题型:选择题
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如右图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为
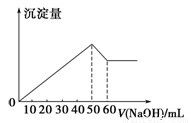
A.6∶1 B.3∶1 C.2∶1 D.1∶2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁实验中学高一上10月阶段测化学试卷(解析版) 题型:选择题
某饱和氯化钠溶液的体积为VmL,密度为ρg/cm3,质量分数为w,物质的量浓度为c mol/L,溶液中所含氯化钠的质量为m g。下列选项正确的是
A.该温度下,氯化钠的溶解度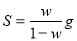
B.溶液中溶质的物质的量浓度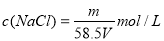
C.溶液中溶质物质的量浓度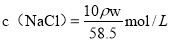
D.溶液中溶质的质量分数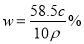
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三10月月考化学试卷(解析版) 题型:填空题
铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示;
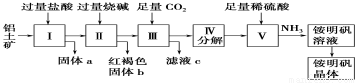
请回答下列问题:
(1)固体a的化学式为__________________,Ⅲ中通入足量CO2气体发生反应的离子方程式为_________________________。
(2)由Ⅴ制取铵明矾溶液的化学方程式为___________________,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)__________________、冷却结晶、过滤洗涤。
(3)以1 000 kg含氧化铝36%的铝土矿为原料制取Al2(SO4)3,需消耗质量分数98%的硫酸(密度1.84 g·cm-1)______________________L(保留4位有效数字)。
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com