
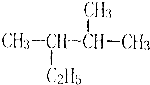 ①2,3一二甲基戊烷;
①2,3一二甲基戊烷;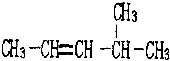 ②4-甲基-2-戊烯.
②4-甲基-2-戊烯. 分析 ①烷烃命名选取最长碳链为主链,从离支链近的一端给主链上的碳原子进行编号.
②烯烃的命名选取含有碳碳双键的最长碳链为主链,距离双键最近的一端命名为1号碳;
解答 解:①烷烃命名选取最长碳链为主链,故主链上有5个碳原子,从离支链近的一端给主链上的碳原子进行编号,则在2号和3号碳原子上各有一个甲基,故名称为:2,3一二甲基戊烷,故答案为:2,3一二甲基戊烷.
②烯烃的命名选取含有碳碳双键的最长碳链为主链,则主链上有5个碳原子,从距离双键最近的一端给主链上的碳原子编号,则双键在2号和3号碳原子之间,在4号碳原子上有一个甲基,故名称为:4-甲基-2-戊烯,故答案为:4-甲基-2-戊烯.
点评 本题主要考查的是烯烃的命名和烷烃的命名,烯烃的命名选取含有碳碳双键的最长碳链,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 向米汤中加入含碘的食盐,观察是否有颜色的变化--检验含碘食盐中是否含碘酸钾 | |
| B. | 向淀粉溶液中加入稀硫酸,加热,再用NaOH中和,并做银镜反应实验--检验淀粉是否水解 | |
| C. | 向甲酸和甲醛的混合物中加入氢氧化钠溶液中和甲酸后,加入新制的氢氧化铜,加热--检验混合物中是否含有甲醛 | |
| D. | 向混有少量乙酸和乙醇杂质的乙酸乙酯中,加入氢氧化钠溶液,然后分液--提纯乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第 VIIA族元素是同周期中非金属性最强的元素 | |
| B. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| C. | 元素周期表中从ⅠA到ⅡB之间12个纵列的元素都是金属元素 | |
| D. | 同周期元素中,ⅠA族元素的原子半径最大(稀有气体除外) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
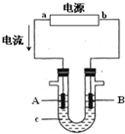 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石 | B. | 石墨 | C. | 铝 | D. | 铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物. ,该化合物含的共价键类型是极性共价键.
,该化合物含的共价键类型是极性共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | Zn+2HCl═ZnCl2+H2↑ | ||
| C. | 2O3$\frac{\underline{\;催化剂\;}}{\;}$3 O2 | D. | CuO+H2$\frac{\underline{\;高温\;}}{\;}$Cu+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com