
| A、非金属原子组成的化合物不可能是离子化合物 |
| B、ⅠA族元素的金属性一定比ⅡA族元素的金属性强 |
| C、同一主族元素组成的化合物一定是共价化合物 |
| D、NH4H中的所有原子的最外层都符合相应稀有气体原子电子层结构,1mol NH5中含有4NA个N-H键(NA表示阿伏加德罗常数的值) |
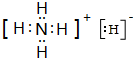 .
.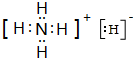 ,根据电子式知,NH4H中的所有原子的最外层都符合相应稀有气体原子电子层结构,且1mol NH5中含有4NA个N-H键(NA表示阿伏加德罗常数的值),故D正确;
,根据电子式知,NH4H中的所有原子的最外层都符合相应稀有气体原子电子层结构,且1mol NH5中含有4NA个N-H键(NA表示阿伏加德罗常数的值),故D正确;

科目:高中化学 来源: 题型:
| 浓H2SO4 |
| 170℃ |
| 浓H2SO4 |
| △ |

| A、①② | B、③④ | C、①③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(B2)=0.01mol?(L?s)-1 |
| B、(C2)=0.002mol?(L?s) -1 |
| C、(D2)=0.006mol?(L?s) -1 |
| D、(A2)=0.008mol?(L?s)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HI与HF的沸点 |
| B、zX和(Z+2)Y的原子半径 |
| C、熟石灰在20℃时与60℃时的溶解度 |
| D、质量分数为20%的氨水与质量分数为10%的氨水的密度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||
B、
| ||||
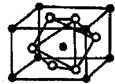
| C、Tl3+核外有6个电子层 | ||||
| D、Tl原子半径大于Cs原子半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L乙烯中含有的原子数为2NA |
| B、1mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
| C、标准状况下,44.8LNO与22.4LO2混合后的气体中含有的分子数为3NA |
| D、常温下,1L0.1mol?L-1 NH4NO3溶液中含有的NH4+和NO3-的总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量的铁与浓硝酸反应:Fe+6H++3NO3-═Fe3++3NO2↑+3H2O |
| B、1mol?L-1的NaAlO2溶液和2.5mol?L-1 的盐酸等体积混合:2AlO2-+5H+═Al(OH)3↓+Al3++H2O |
| C、在碳酸氢镁溶液中加入足量 Ca(OH)2 溶液:Mg2++2HCO3-+Ca2++2OH-═MgCO3↓+CaCO3↓+2H2O |
| D、H2O中投入Na218O2固体:2H2O+218O22-═418OH-+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 为了控制燃煤电厂所排放的烟气中氮氧化物,目前常采用选择性催化还原法(SCR)进行脱硝.在其脱硝过程中,V2O5-WO3/TiO2催化剂是决定脱硝效率的关键因素.该催化剂随温度的升高其活性会下降,若在反应前期通入SO2,在催化剂表面氧化并最终形成硫酸,增强了催化剂表面的酸性,从而提高了高温下催化剂的活性,根据以上信息,回答问题:
为了控制燃煤电厂所排放的烟气中氮氧化物,目前常采用选择性催化还原法(SCR)进行脱硝.在其脱硝过程中,V2O5-WO3/TiO2催化剂是决定脱硝效率的关键因素.该催化剂随温度的升高其活性会下降,若在反应前期通入SO2,在催化剂表面氧化并最终形成硫酸,增强了催化剂表面的酸性,从而提高了高温下催化剂的活性,根据以上信息,回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 喀麦隆的“杀人湖”(尼奥斯湖)曾于1986年使1800多名附近居民在一夜之间神秘死去.后经科学家考察发现,湖底有火山口,聚集了大量二氧化碳和二氧化硫等有毒气体并发现在200m深的湖底,每立方米湖水竟溶解8m3的有毒气体,目前科技人员已找到一种有效的办法将湖底的有毒气体抽出并加以处理.回答:
喀麦隆的“杀人湖”(尼奥斯湖)曾于1986年使1800多名附近居民在一夜之间神秘死去.后经科学家考察发现,湖底有火山口,聚集了大量二氧化碳和二氧化硫等有毒气体并发现在200m深的湖底,每立方米湖水竟溶解8m3的有毒气体,目前科技人员已找到一种有效的办法将湖底的有毒气体抽出并加以处理.回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com