
【题目】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ① | |||||||
二 | ② | ③ | ④ | |||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在标号元素中,最活泼的金属元素是____。最活泼的非金属元素是____。(写元素符号)⑨元素的离子结构示意图是____________________。
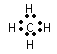
(2)①与②形成共价化合物的电子式 _______________。用电子式表示⑤与⑨形成化合物的形成过程__________________________________________。
(3)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是________。(写元素符号)
(4)⑦、⑧、⑨三种元素所形成的气态氢化物中,最稳定的氢化物是____(写分子式);其三种元素的最高价含氧酸的酸性由强到弱的顺序 _________。(写酸的分子式)
(5)写出⑥元素的单质与氢氧化钠反应的离子方程式:____________________。
【答案】 Na F 
![]() Na>Al>Si HCl HClO4> H3PO4> H2SiO3 2Al + 2OH- +2H2O = 2AlO2- + 3H2↑
Na>Al>Si HCl HClO4> H3PO4> H2SiO3 2Al + 2OH- +2H2O = 2AlO2- + 3H2↑
【解析】根据元素在周期表中的位置可知,①为H元素,②为C元素,③为O元素,④为F元素,⑤为Na元素,⑥为Al元素,⑦为Si元素,⑧为P元素,⑨为Cl元素。
(1)根据元素的金属性和非金属性的变化规律,同一周期,从左到右,金属性逐渐减弱,非金属性逐渐增强,同一主族,从上到下,金属性逐渐增强,非金属性逐渐减弱,最活泼的金属元素是钠。最活泼的非金属元素是氟。氯为17号元素,离子结构示意图为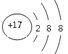 ,故答案为:Na ;F;
,故答案为:Na ;F; ;
;
(2)①与②形成共价化合物可以为甲烷,电子式为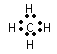 。⑤与⑨形成化合物为氯化钠,属于离子化合物,用电子式表示氯化钠的形成过程为
。⑤与⑨形成化合物为氯化钠,属于离子化合物,用电子式表示氯化钠的形成过程为![]() ,故答案为:
,故答案为: ;
; ![]() ;
;
(3)同一周期,从左到右,原子半径逐渐减小,⑤、⑥、⑦三种元素的原子半径由大到小的顺序为Na>Al>Si,故答案为:Na>Al>Si;
(4) 同一周期,从左到右,非金属性逐渐增强,非金属性越强,氢化物越稳定,⑦、⑧、⑨三种元素所形成的气态氢化物中,最稳定的氢化物是HCl;非金属性越强,最高价含氧酸的酸性越强,三种元素的最高价含氧酸的酸性由强到弱的顺序为HClO4> H3PO4> H2SiO3,故答案为:HCl;HClO4> H3PO4> H2SiO3;
(5)铝与氢氧化钠反应的离子方程式为2Al + 2OH- +2H2O = 2AlO2- + 3H2↑,故答案为:2Al + 2OH- +2H2O = 2AlO2- + 3H2↑。


科目:高中化学 来源: 题型:
【题目】下列实验中,所采取的分离方法不正确的是( )
选项 | 目的 | 分离方法 |
A | 除去铜器表面的铜绿[Cu2(OH)2CO3] | 用盐酸浸泡,再用清水冲洗 |
B | 除去乙醇中的少量水 | 加生石灰,再蒸馏 |
C | 除去氯化铁中含有少量氯化亚铁杂质 | 加入溴水 |
D | 除去NaCl固体中的NH4Cl | 加热 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是
A. 苯与浓硝酸、浓硫酸共热并保持50-60℃反应生成硝基苯
B. 乙烷与氯气在铁粉作用下生成一氯乙烷
C. 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷
D. 煤经过气化和液化等化学变化可以转化为清洁燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaTiO3的晶体结构模型如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角),下列关于晶体的说法正确的是( )

A. CaTiO3的摩尔质量为236
B. CaTiO3晶体中每个Ti4+与12个Ca2+紧相邻
C. CaTiO3晶体中每个Ti4+与12个O2-紧相邻
D. CaTiO3晶体中每个Ti4+与12个Ti4+紧相邻
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是

A. 含有大量SO42-的溶液中肯定不存在Ag+
B. 0.02 mol·L-1的AgNO3溶液与0.02 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀
C. Ag2SO4的溶度积常数(Ksp)为1×10-3
D. a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X中可能含有Fe2+、A13+、NH4+、CO32-、SO32-、SO42-、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如下,下列说法不正确的是

A. X 中肯定存在 Fe2+、A13+、NH4+、SO42-
B. X中不能确定是否存在的离子是Al3+和Cl-
C. 溶液E和气体F发生反应,生成物为盐类
D. 气体A是NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年春节,京津冀及周边区域遭遇“跨年”雾霾,二氧化硫、氮氧化物以及可吸入颗粒物这三项是雾霾主要组成,消除氮氧化物污染是研究方向之一。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574.0 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160.0 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1
请写出CH4(g)与NO2(g)反应生成N2(g) ,CO2(g)和H2O(l)的热化学方程式_______________________ 。
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g)![]() N2(g)+CO2(g),某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T0C)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g),某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T0C)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度(mol/L) 时间(min) | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
①下列说法不能作为判断该反应达到化学平衡状态标志的是_______
A.活性炭的质量 B.v 正(N2) = 2v逆 (NO)
C.容器内压强保持不变 D.容器内混合气体的密度保持不变
E.容器内混合气体的平均相对分子质量保持不变
F.容器内CO2的浓度保持不变
②在T0C时,该反应的平衡常数为______________(小数点后保留两位有效数字);
③在30 min时,若只改变某一条件,反应重新达到平衡,则改变的条件是___________;
④在50 min时保持温度和容器体积不变再充入NO和N2,使二者的浓度均增加至原来的两倍,则化学平衡_______(填“正向移动”、“逆向移动”或“不移动”)
(3)利用反应6NO2+8NH3= 7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。

①A电极的电极反应式为______________
②下列关于该电池的说法正确的是(_____)
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一断时间,溶液的pH不变
D.当有4.48LNO2被处理时,转移电子物质的量为0.8mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com