
��16�֣�ֱ���ŷ�úȼ�ղ������������������صĻ������⣬������ͨ��װ��ʯ��ʯ��Һ������װ�ÿ��Գ�ȥ���еĶ�������������������ơ�����ƿ�����ͼ��ʾ��ѭ��ȼ��װ�õ�ȼ�Ϸ�Ӧ��������鷴Ӧ�������������ˮ��õ������������ʵĶ�����̼���Ӷ������ڶ�����̼�Ļ������ã��ﵽ����̼�ŷŵ�Ŀ�ġ�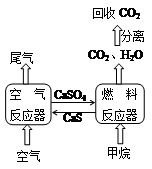
��ش��������⣺
��1��úȼ�ղ���������ֱ���ŷŵ������У���������Ҫ���������� ������д��ĸ��ţ�
| A������ЧӦ | B������ | C���۳���Ⱦ | D��ˮ�帻Ӫ���� |
 ��
��
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
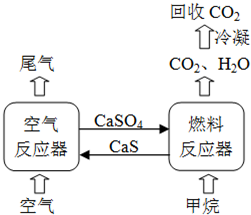 ��2012?�Ĵ���ֱ���ŷ�úȼ�ղ������������������صĻ������⣬������ͨ��װ��ʯ��ʯ��Һ������װ�ÿ��Գ�ȥ���еĶ�������������������ƣ�����ƿ�����ͼ��ʾ��ѭ��ȼ��װ�õ�ȼ�Ϸ�Ӧ��������鷴Ӧ�������������ˮ��õ������������ʵĶ�����̼���Ӷ������ڶ�����̼�Ļ������ã��ﵽ����̼�ŷŵ�Ŀ�ģ�
��2012?�Ĵ���ֱ���ŷ�úȼ�ղ������������������صĻ������⣬������ͨ��װ��ʯ��ʯ��Һ������װ�ÿ��Գ�ȥ���еĶ�������������������ƣ�����ƿ�����ͼ��ʾ��ѭ��ȼ��װ�õ�ȼ�Ϸ�Ӧ��������鷴Ӧ�������������ˮ��õ������������ʵĶ�����̼���Ӷ������ڶ�����̼�Ļ������ã��ﵽ����̼�ŷŵ�Ŀ�ģ� ��
��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ���������У�����������������ۻ�ѧ�Ծ��������棩 ���ͣ������
2013������������������Ű������ȵ��������У�ȼú������β������ɿ�����Ⱦ��ԭ��֮һ��
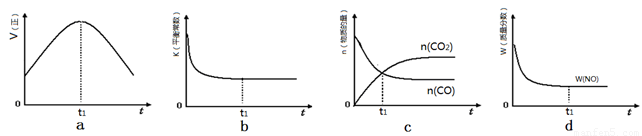
��1������β����������Ҫԭ��Ϊ��2NO(g) + 2CO(g)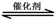 2CO2(g)+ N2(g)����H��0
2CO2(g)+ N2(g)����H��0
�ٸ÷�Ӧƽ�ⳣ������ʽ
�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬���� ������ţ���
��2��ֱ���ŷ�úȼ�ղ������������������صĻ������⡣
úȼ�ղ����������������������CH4����ԭNOX�������������������Ⱦ��
��֪��CH4(g)+2NO2(g)��N2(g)��CO2(g)+2H2O(g)�� ��H����867 kJ/mol
2NO2(g)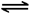 N2O4(g)
��H����56.9 kJ/mol
N2O4(g)
��H����56.9 kJ/mol
H2O(g) �� H2O(l) ��H �� ��44.0 kJ��mol
д��CH4����ԭN2O4(g)����N2��H2O(l)���Ȼ�ѧ����ʽ�� ��
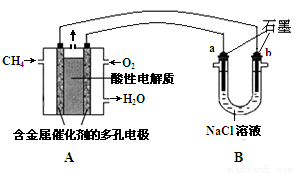
��3������ȼ�ϵ�ؿ����������������ʡ���ͼ�����ü���ȼ�ϵ�ص��100mL1mol/Lʳ��ˮ,���һ��ʱ����ռ�����״���µ�����2.24L���������Һ������䣩.
�ټ���ȼ�ϵ�صĸ�����Ӧʽ�� ��
�ڵ�����Һ��pH= (��������������������Һ��Ӧ)
�������������������ڱ�״������ L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012����ͨ�ߵ�ѧУ����ȫ��ͳһ�������ۻ�ѧ���֣��Ĵ��������棩 ���ͣ������
��16�֣�ֱ���ŷ�úȼ�ղ������������������صĻ������⣬������ͨ��װ��ʯ��ʯ��Һ������װ�ÿ��Գ�ȥ���еĶ�������������������ơ�����ƿ�����ͼ��ʾ��ѭ��ȼ��װ�õ�ȼ�Ϸ�Ӧ��������鷴Ӧ�������������ˮ��õ������������ʵĶ�����̼���Ӷ������ڶ�����̼�Ļ������ã��ﵽ����̼�ŷŵ�Ŀ�ġ�
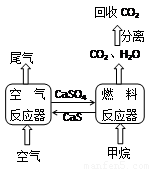
��ش��������⣺
��1��úȼ�ղ���������ֱ���ŷŵ������У���������Ҫ���������� ������д��ĸ��ţ�
A������ЧӦ B������ C���۳���Ⱦ D��ˮ�帻Ӫ����
��2������������Ĺ����У����õ�ʯ��ʯ��Һ�ڽ�������װ��ǰ����ͨһ��ʱ�������̼������������Ч�ʣ�����ʱ���ƽ�Һ��pHֵ����ʱ��Һ���е���������ƿ��Ա���������������������ơ�
�ٶ�����̼��ʯ��ʯ��Һ��Ӧ�õ��IJ���Ϊ ��
����������Ʊ���������������������ƵĻ�ѧ����ʽΪ ��
��3����֪1mol CH4��ȼ�Ϸ�Ӧ������ȫ��Ӧ������̬ˮʱ���� 160.1kJ��1mol CH4����������ȫȼ��������̬ˮʱ����802.3kJ��д��������Ӧ���з������Ȼ�ѧ����ʽ�� ��
��4�����յ�CO2�뱽������һ��������Ӧ�����л���M���仯ѧʽΪC7H5O3Na��M��ϡ�����ữ��õ�һ��ҩ���м���N��N�Ľṹ��ʽΪ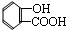 ��
��
��M�Ľṹ��ʽΪ ��
�ڷ������ޡ�O��O����ȩ���뱽��ֱ��������N��ͬ���칹�干�� �֡�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com