
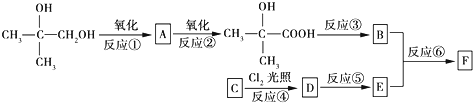
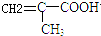 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$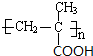 .
. .
.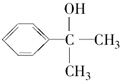 .
. 分析 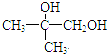 催化氧化生成A,A催化氧化生成
催化氧化生成A,A催化氧化生成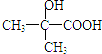 ,则A为
,则A为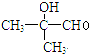 ;
;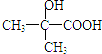 发生反应生成B,B和E通过反应生成芳香酯类物质F( C11H12O2),则E为含有7个C醇,只能为
发生反应生成B,B和E通过反应生成芳香酯类物质F( C11H12O2),则E为含有7个C醇,只能为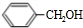 ,故C为
,故C为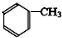 ,C与氯气在光照条件下发生取代反应生成D,则D为
,C与氯气在光照条件下发生取代反应生成D,则D为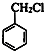 ;结合F的分子式可知F为
;结合F的分子式可知F为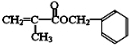 ,则
,则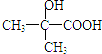 发生消去反应生成B为
发生消去反应生成B为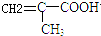 ,据此解答.
,据此解答.
解答 解: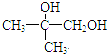 催化氧化生成A,A催化氧化生成
催化氧化生成A,A催化氧化生成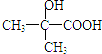 ,则A为
,则A为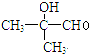 ;
;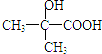 发生反应生成B,B和E通过反应生成芳香酯类物质F( C11H12O2),则E为含有7个C醇,只能为
发生反应生成B,B和E通过反应生成芳香酯类物质F( C11H12O2),则E为含有7个C醇,只能为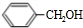 ,故C为
,故C为 ,C与氯气在光照条件下发生取代反应生成D,则D为
,C与氯气在光照条件下发生取代反应生成D,则D为 ;结合F的分子式可知F为
;结合F的分子式可知F为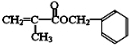 ,则
,则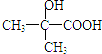 发生消去反应生成B为
发生消去反应生成B为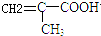 .
.
(1)A为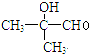 ,含有的官能团为羟基和醛基;根据分析可知,反应③为消去反应、反应④为取代反应,反应⑤为取代反应,反应⑥是酯化反应,也属于取代反应,所以属于取代反应的为:②③④,
,含有的官能团为羟基和醛基;根据分析可知,反应③为消去反应、反应④为取代反应,反应⑤为取代反应,反应⑥是酯化反应,也属于取代反应,所以属于取代反应的为:②③④,
故答案为:羟基、醛基;④⑤⑥;
(2)C为 ,其名称为甲苯;反应③为
,其名称为甲苯;反应③为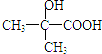 发生消去反应生成的
发生消去反应生成的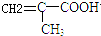 ,反应条件为浓硫酸、加热,
,反应条件为浓硫酸、加热,
故答案为:甲苯;浓硫酸、加热;
(3)B为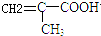 ,分子中含有碳碳双键,能够发生加聚反应生成高分子化合物,该反应的化学方程式为:n
,分子中含有碳碳双键,能够发生加聚反应生成高分子化合物,该反应的化学方程式为:n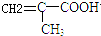 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$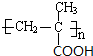 ,
,
故答案为:n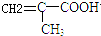 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$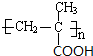 ;
;
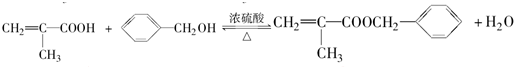
(4)反应⑥的化学方程式为: ,
,
故答案为: ;
;
(5)A为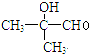 、B为
、B为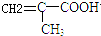 、E为
、E为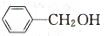 ,溴水与A、B的反应现象相同;酸性高锰酸钾都能够与三种有机物反应;溴的四氯化碳溶液都能够与A、B反应,只有a.新制的Cu(OH)2浊液能够鉴别:与A能够发生氧化还原反应生成砖红色沉淀、与B发生正反应,浊液变澄清、与E不反应,
,溴水与A、B的反应现象相同;酸性高锰酸钾都能够与三种有机物反应;溴的四氯化碳溶液都能够与A、B反应,只有a.新制的Cu(OH)2浊液能够鉴别:与A能够发生氧化还原反应生成砖红色沉淀、与B发生正反应,浊液变澄清、与E不反应,
故答案为:a;
(6)E为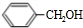 ,G是E的同系物且相对分子质量比E大28,G比E多2个CH2原子团,说明G分子中含有1个苯环、醇羟基,且侧链含有3个C原子,有1个侧链,可以看作丙烷中2个氢原子被苯基、-OH取代,有5种,有2个侧链为-CH3、CH2CH2OH,或-CH3、-CH(OH)2CH3,或者-CH2CH3、-CH2OH,各有邻、间、对3种,有3个侧链为2个-CH3、1个-CH2OH,2个-CH3处于邻位,-CH2OH有2种位置,2个-CH3处于间位,-CH2OH有3种位置,2个-CH3处于对位,-CH2OH有1种位置,共有20种,其中核磁共振氢谱有5组峰,且面积比为6:2:2:1:1的结构简式为
,G是E的同系物且相对分子质量比E大28,G比E多2个CH2原子团,说明G分子中含有1个苯环、醇羟基,且侧链含有3个C原子,有1个侧链,可以看作丙烷中2个氢原子被苯基、-OH取代,有5种,有2个侧链为-CH3、CH2CH2OH,或-CH3、-CH(OH)2CH3,或者-CH2CH3、-CH2OH,各有邻、间、对3种,有3个侧链为2个-CH3、1个-CH2OH,2个-CH3处于邻位,-CH2OH有2种位置,2个-CH3处于间位,-CH2OH有3种位置,2个-CH3处于对位,-CH2OH有1种位置,共有20种,其中核磁共振氢谱有5组峰,且面积比为6:2:2:1:1的结构简式为 ,
,
故答案为:20; .
.
点评 本题考查了有机推断,熟练掌握官能团的性质与衍变,试题充分考查了学生的分析推理能力及灵活应用基础知识的能力,(6)中同分异构体书写为难点、易错点,需要掌握同分异构体的书写原则,难度中等.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 镁、铝的熔点很高,可用于制耐火坩埚 | |
| B. | 小苏打受热分解生成气体,可用作发酵粉 | |
| C. | 铁的活泼性较强,铁粉可用作食品袋内的脱氧剂 | |
| D. | Na、Cu等金属化合物焰色反应呈现各种艳丽色彩,可制成节日烟花 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 方程式 | 结论 |
| A | 2AgI(s)+S2-(aq)?Ag2S(s)+2I-(aq) | 溶解度:Ag2S>AgI |
| B | C(s.石墨)═C(s.金刚石)△H>0 | 稳定性:金刚石>石墨 |
| C | 3Fe2++NO${\;}_{3}^{-}$+10H+═3Fe3++3H2O+NH${\;}_{4}^{+}$ | 还原性:Fe2+>NH${\;}_{4}^{+}$ |
| D | 2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3;Fe+S$\frac{\underline{\;加热\;}}{\;}$FeS | 氧化性:Cl2>S |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和氯化铁溶液反应:Fe3++Fe═2Fe2+ | |
| B. | 醋酸和氢氧化钠溶液反应:CH3COOH+OH-═CH3COO-+H2O | |
| C. | 实验室用MnO2和浓盐酸制取Cl2:MnO2+2H++2Cl-═Mn2++Cl2↑+H2O | |
| D. | 氢氧化铁和盐酸反应:H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 | |
| B. | 钢铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| C. | 绿色化学的核心是从源头上消除工业生产对环境的污染 | |
| D. | 汽油、柴油和植物油都是碳氢化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 电浮选凝聚法是工业上采用的一种污水处理方法,即保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,Fe(OH)3胶体具有吸附作用,可吸附水中的污物而使其沉淀下来,起到净水的作用,其原理如图所示.下列说法正确的是( )
电浮选凝聚法是工业上采用的一种污水处理方法,即保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,Fe(OH)3胶体具有吸附作用,可吸附水中的污物而使其沉淀下来,起到净水的作用,其原理如图所示.下列说法正确的是( )| A. | 石墨电极上发生氧化反应 | |
| B. | 根据图示,物质A为CO2 | |
| C. | 为增强污水的导电能力,可向污水中加入适量乙醇 | |
| D. | 甲烷燃料电池中CO32-向空气一极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
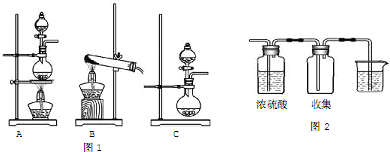
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
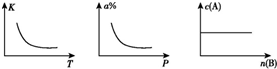
| A. | m+n<p,△H>0 A、B、C均为气体 | B. | m<p△H<0 A、C均为气体 | ||
| C. | n>p,△H>0 B、C均为气体 | D. | m>p,△H<0 A、C均为气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com