
许多物质的氧化能力受溶液酸碱性的影响。高锰酸钾在不同的条件下发生的还原反应如下:
MnO4—+ 5e + 8H+ → Mn2+ + 4H2O
MnO4— + 3e + 2H2O → MnO2 + 4OH—
MnO4— + e → MnO42—(溶液呈绿色)
MnO2的还原反应可表示如下:MnO2+4H+ + 2e → Mn2++2H2O
(1)MnO2与稀盐酸不能制取氯气,其原因是 。
(2)将SO2通入KMnO4溶液中,发生还原反应的过程为______→_______
(用化学式或离子符号表示)。
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列叙述正确的是________(选填编号)。
a.氧化性:PbO2>KMnO4 b.还原性:PbO2> KMnO4
c.该反应可以用盐酸酸化
(4)将高锰酸钾溶液逐滴加入到硫化钾溶液中可发生如下反应,其中K2SO4和S的物质的量之比为3:2。完成并配平该反应的化学方程式。
___KMnO4+___K2S+___ _____ → ___K2MnO4 +___K2SO4 +__S↓+___ ___
反应若生成5.44 g单质硫,反应过程中转移电子的物质的量为__________。
(1)MnO2在酸性较强的环境中才有制取氯气的氧化能力。( 1分)
(2)MnO4—→ Mn2+(2分)
(3)a (1分)
(4)28 5 24KOH 28 3 2 12H2O(2分);2.38mol(2分)
解析试题分析:(1)MnO2与稀盐酸不能制取氯气,其原因是MnO2在酸性较强的环境中才有制取氯气的氧化能力。
(2)将SO2通入KMnO4溶液中,发生还原反应的过程即为化合价降低的过程,为MnO4—→ Mn2+。
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色,说明有酸性高锰酸钾生成,说明氧化性:PbO2>KMnO4。
(41)根据氧化还原反应原理和K2SO4和S的物质的量之比为3:2。该反应的化学方程式28KMnO4+5_K2S+24KOH → __28K2MnO4 +_3_K2SO4 +_2S↓+_12H2O,根据 2S----28e-关系式,可以求出反应若生成5.44 g单质硫,反应过程中转移电子的物质的量为2.38mol。
考点:考查氧化还原的配平和计算以及氧化性强弱的判断。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:填空题
Ⅰ.某实验A小组设计生产亚氯酸钠(NaClO2)的主要流程如图,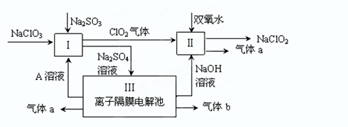
已知NaClO2是一种强氧化性漂白剂,广泛用于纺织、印染工业。它在碱性环境中稳定存在。
(1)双氧水的电子式为 ,装置Ⅰ中发生反应的还原剂是 (填化学式)。
(2)A的化学式是 ,装置Ⅲ电解池中A在 极区产生,若装置Ⅲ中生成气体a为 11.2 L(标准状况),则理论上通过电解池的电量为 (已知法拉第常数F="9.65×l" 04C· mol-1)。
(3)装置Ⅱ中反应的离子方程式是 。
Ⅱ.某实验B小组测定金属锡合金样品的纯度(仅含少量锌和铜,组成均匀),将样品溶于足量盐酸: Sn+ 2HCl=SnCl2+H2↑,过滤,洗涤。将滤液和洗涤液合并再加过量的FeCl3溶液。最后可用一定浓度的K2Cr2O7酸性溶液滴定生成的Fe2+,此时还原产物为Cr3+。现有锡合金试样1.23g,经上述反应、操作后,共用去0.200mol/L的K2Cr2O7的酸性溶液15.00mL。
(4) 列式计算样品中锡的质量分数。
(5)用上述样品模拟工业上电解精炼锡,如图: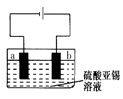
b极发生电极反应式 ,当得到11.90g纯锡时,电解质溶液质量减轻0.54g,则锡合金质量减少_______ g(结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
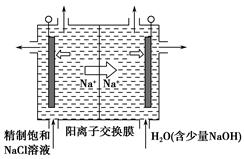
(1)工业上制备ClO2的反应原理为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①浓盐酸在反应中显示出来的性质是________。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
实验室可用KMnO4固体和浓盐酸反应制氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓) =2KCl+2MnCl2+5Cl2↑+8H2O。
(1)该反应中氧化剂是_____________,还原剂是__________________。
(2)若反应中有0.20 mol 电子发生转移,生成氯气的体积为 (标准状况),被氧化的HCl的物质的量是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数 (25℃) | 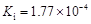 |  | 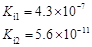 | 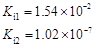 |
 ,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下:
,但它的氧化性比硫酸还要强。在酸性介质中,碲酸可将HI氧化成I2,方程式如下: TeO2+ Te+ I2+ H2O
TeO2+ Te+ I2+ H2O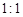 ,试配平上述化学方程式。
,试配平上述化学方程式。查看答案和解析>>
科目:高中化学 来源: 题型:填空题
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
请同答下列问题:
(l)写出向KOH溶液中通入足量Cl2发生反应的离子方程式_______ 。
(2)在溶液I中加入KOH固体的目的是______(填编号)。
| A.为下一步反应提供碱性的环境 |
| B.使KClO3转化为KClO |
| C.与溶液I中过量的Cl2继续反应,生成更多的KClO |
| D.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(6分)下列反应原理可以用于检查司机是否酒后开车。
K2Cr2O7+C2H5OH+H2SO4—Cr2(SO4)3+CH3COOH+K2SO4+
(1)在反应中,氧化剂是 。如果在反应中生成1molCr3+,转移电子数为 。(用NA表示阿伏加德罗常数)
(2)写出上述化学方程式所缺项(填化学式) 。
(3)乙醇(C2H5OH)和乙醚(CH3CH2OCH2CH3)的沸点分别是78.5℃、34.5℃,分离二者混合物的方法是 ,乙醇比乙醚的沸点高的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
KClO3和浓HCl在一定温度下反应会生成黄绿色的易爆物二氧化氯。其反应可表述为:
KClO3+ HCl(浓)= KCl+ ClO2+ Cl2+ H2O
(1)配平以上化学方程式(化学计量数填入划线上)并用双线桥标出电子转移的方向和数目。
(2)反应中的氧化剂是 , ClO2是反应的 (填氧化或还原)产物。
(3)反应产生0.1 mol Cl2,则转移的电子的物质的量为 mol。
(4)ClO2具有很强的氧化性,因此可被用来做消毒剂,若ClO2作消毒剂后其自身转化为Cl-,则其消毒的效率(以单位物质的量得到电子数表示)是Cl2的 倍。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究过氧化氢的性质。
请填写下列空白:
(1)移取10.00 mL密度为ρg·mL-1的过氧化氢溶液至250 mL________(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。 MnO4-+
MnO4-+ H2O2+
H2O2+ H+=
H+= Mn2++
Mn2++ O2+
O2+
(3)滴定时,将高锰酸钾标准溶液注入____________(填“酸式”或“碱式”)滴定管中。
如何判断滴定到达终点:
。
(4)如图表示25 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填序号)________。
| A.是a mL | B.是(25-a)mL | C.一定大于a mL | D.一定大于(25-a)mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com