
| 29a |
| 37 |
| 29a |
| 37 |
| 1.76g |
| 44g/mol |
| 0.36g |
| 18mol |
| 0.96g |
| 16g/mol |
| 1.76g |
| 44g/mol |
| 1.48g |
| 148g/mol |
| 0.336L |
| 22.4L/mol |
| a g |
| 148g/mol |
| a g |
| 148g/mol |
| 29a |
| 37 |
| 29a |
| 37 |


科目:高中化学 来源: 题型:
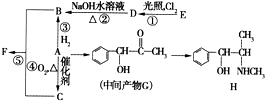 有机物A是重要的化工合成原料,在医药、染料和香料等行业有着广泛的应用.由A制得某药物H的转化关系如图所示(A→G、G→H的反应条件和部分反应物已略去).
有机物A是重要的化工合成原料,在医药、染料和香料等行业有着广泛的应用.由A制得某药物H的转化关系如图所示(A→G、G→H的反应条件和部分反应物已略去).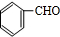


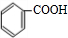 +
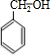
+
| 浓硫酸 |
| △ |
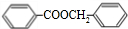 +H2O
+H2O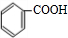 +
+
| 浓硫酸 |
| △ |
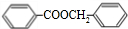 +H2O
+H2O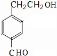

查看答案和解析>>
科目:高中化学 来源: 题型:









查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A是重要的合成原料,在医药、染料、香料等行业有着广泛的应用。由A可以制得麻黄碱和其他很多物质。现有如下转化关系图(略去了由A→G,G→麻黄碱的部分反应物和条件):
请回答下列问题:
(1)关于麻黄碱下列说法正确的是 (填字母)。
a.麻黄碱的分子式为C10H15NO
b.1mol麻黄碱可以对应消耗1molHCl或NaOH
c.麻黄碱可以发生消去和酯化反应
d.麻黄碱属于芳香烃
(2)已知有机物A的相对分子质量为106,A中含碳、氢、氧的质量之比为42:3:8,
则A的含氧官能团名称是 ;检验该官能团的实验是 。
(3)反应①~⑤中属于取代反应的是 (填序号)。
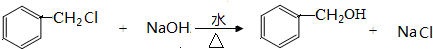
(4)写出D—B的化学方程式 。
(5)F可作多种香精的定香剂,请写出B和C反应生成F的化学方程式 。
(6)写出符合下列条件的同分异构体的结构简式 。
①与中间产物G互为同分异构体
②既能发生消去反应,又能发生酯化反应
③苯环上的一氯取代物只有两种,分子结构中没有甲基
(7)已知:
|
| 溶解性 | 沸点 |
| A | 微溶于水 | 179.0℃ |
| E | 不溶于水 | 110.8℃ |
A可以由E制取,制取工艺中得到的是A、E混合物,分离该混合物的方法是 。
查看答案和解析>>
科目:高中化学 来源:2011届贵州省遵义四中高三上学期第四次月考(理综)化学部分 题型:实验题
有机物A是重要的合成原料,在医药、染料、香料等行业有着广泛的应用。由A可以制得麻黄碱和其他很多物质。现有如下转化关系图(略去了由A→G,G→麻黄碱的部分反应物和条件):
请回答下列问题:
(1)关于麻黄碱下列说法正确的是 (填字母)。
a.麻黄碱的分子式为C10H15NO
b.1mol麻黄碱可以对应消耗1molHCl或NaOH
c.麻黄碱可以发生消去和酯化反应
d.麻黄碱属于芳香烃
(2)已知有机物A的相对分子质量为106,A中含碳、氢、氧的质量之比为42:3:8,
则A的含氧官能团名称是 ;检验该官能团的实验是 。
(3)反应①~⑤中属于取代反应的是 (填序号)。
(4)写出D—B的化学方程式 。
(5)F可作多种香精的定香剂,请写出B和C反应生成F的化学方程式 。
(6)写出符合下列条件的同分异构体的结构简式 。
①与中间产物G互为同分异构体
②既能发生消去反应,又能发生酯化反应
③苯环上的一氯取代物只有两种,分子结构中没有甲基
(7)已知:
| | 溶解性 | 沸点 |
| A | 微溶于水 | 179.0℃ |
| E | 不溶于水 | 110.8℃ |
查看答案和解析>>
科目:高中化学 来源:09-10年西南师大附中高二下期期末考试化学卷 题型:计算题
(8分) 已知有机物A的相对分子质量不超过200。取1.48 g A完全燃烧后,将燃烧产物通过碱石灰,碱石灰的质量增加2.12g;若将燃烧产物通过浓硫酸,浓硫酸的质量增加0.36 g;取1.48 g A与足量钠反应,生成的气体在标准状况下的体积为0.336L。
(1) 1.48 g A完全燃烧生成的CO2的物质的量为________mol。
(2) A的分子式为_______________。
(3) A能使紫色石蕊试液变红,且A经催化氧化后分子中只有一种氢原子,则A的结构简式为_____________。
(4) 将a g A完全燃烧后的产物全部通入足量的Na2O2固体充分吸收,则固体质量增加
____________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com