
【题目】在标准状况下,将O2与NO2按3:4的体积比充满一个干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升后,最后烧瓶内溶液的物质的量浓度约为( )
A.0.045mol·L-1 B.0.036mol·L-1 C.0.026mol·L-1 D.0.030mol·L-1
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | R |
利用表中元素回答下列问题:
(1)X元素在周期表中的位置为__________。
(2)气态氢化物水溶液呈碱性的元素是_____________,此氢化物的电子式__________。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是__________。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)![]() 和
和![]() 是元素R的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为w g,则
是元素R的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为w g,则![]() 的相对原子质量的表达式为___________,元素R的相对原子质量的表达式为______________________。
的相对原子质量的表达式为___________,元素R的相对原子质量的表达式为______________________。
(5)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/L NaOH溶液和1mol O2,则两种气体中相对分子质量较大的气体的分子式及物质的量为__________、_____________,生成硫酸铜的物质的量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁是一种性质活泼的金属,请回答下列问题:
(1)甲组同学通过实验探究Mg能否在CO2气体中燃烧,将镁条在空气中点燃后迅速插入盛有CO2气体的集气瓶中,观察到镁条剧烈燃烧,瓶内壁出现黑色固体颗粒等现象。写出Mg在CO2中燃烧的化学方程式:__________
(2)乙组同学根据甲组实验,推测Mg也能在NO2中燃烧,可能产物为MgO 、Mg3N2、和N2。请通过下图所给装置及药品来验证反应产物(夹持装置省略,部分仪器可重复使用)。
已知:a. Mg3N2遇水强烈水解。
b. NO2气体能被NaOH吸收。
c.25℃时,电离常数:CH3COOH的Ka=1.8×10-5 NH3·H2O的Ka=1.8×10-5

回答下列问题:
①乙组同学实验装置连接的正确顺序为A→__________(填装置字母);装置C中盛放的试剂是________。
②当实验过程中出现_________现象时,才能开始加热,确定产物中有N2生成的实验现象为_________。
③装置D中生成两种物质的量相等的钠盐,其离子方程式为___________。
(3)设计实验证明:
①产物中存在Mg3N2:__________________。
②Mg(OH)2与NH4+直接反应而溶解:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
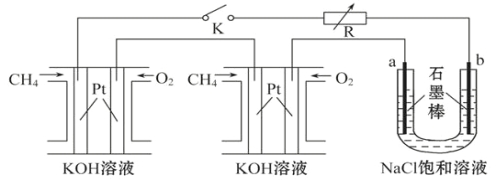
回答下列问题:
(1)甲烷燃料电池正极的电极反应为________________、负极的电极反应____________。
(2)闭合K开关后,a、b电极上均有气体产生,其中b电极上得到的是____________,电解氯化钠溶液的总反应方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应A+3B2C+D在某段时间内以A的浓度变化表示的化学反应速度为1molL﹣1min﹣1 , 则此段时间内以C的浓度变化表示的化学反应速率为( )
A.0.5molL﹣1min﹣1
B.1molL﹣1min﹣1
C.2molL﹣1min﹣1
D.3molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验以探究元素性质的递变规律,实验装置如图所示:
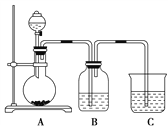
实验Ⅰ:根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律。
已知A装置的烧瓶里装有大理石,分液漏斗里装有稀HNO3,B装置中装有饱和碳酸氢钠溶液,C装置中装有Na2SiO3溶液,试回答:
(1)A中反应的离子方程式为____________,C中可观察到的现象是________。
(2)B装置的作用是______________。
(3)根据实验现象推知,碳酸、硝酸、原硅酸的酸性强弱顺序是________,由此得出碳、氮、硅三种元素非金属性的强弱顺序是________________。
实验Ⅱ:已知常温下高锰酸钾与浓盐酸混合可产生氯气,利用该装置探究氯元素和溴元素的非金属性强弱。
(4)写出B装置中发生反应的离子方程式:__________________________。
(5)C装置的作用是_______________________。
(6)实验结论:氧化性:________,非金属性:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com