
(4分)对反应2 KMnO4 + 16 HCl = 2 KCl + 2 MnCl2 + 5Cl2 ↑ +8 H2O完成
下列问题:
在此化学反应中_________是氧化剂,__________是氧化产物。若有1.6摩尔HCl参加反应,则有 摩尔电子转移。
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
(2011?昌平区二模)下列实验中,能够达到预期目的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
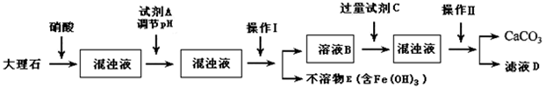
 ,溶液变红色,说明滤液中含Fe3+
,溶液变红色,说明滤液中含Fe3+ ,溶液变红色,说明滤液中含Fe3+
,溶液变红色,说明滤液中含Fe3+查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| KMnO4酸性溶液 的浓度/mol?L-1 |
溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | T/K | c(Na2S2O3)/mol?L-1 | c(H2SO4)/mol?L-1 | 实验目的 |
| ① | 298 | 0.1 | 0.1 | 实验①和②探究温度对该反应速率的影响;实验①、③和④探究反应物浓度对该反应速率的影响 |
| ② | 308 | |||
| ③ | 0.2 | |||
| ④ | 0.1 |
| O | 2- 4 |
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体于试管中,加蒸馏水溶解 | |
| 步骤2: | |
| 步骤3: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com