
【题目】工业上可由乙苯生产苯乙烯: ![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.该反应的类型为消去反应
B.乙苯的同分异构体共有三种
C.可用Br2、CCl4鉴别乙苯和苯乙烯
D.乙苯和苯乙烯分子内共平面的碳原子数均为7
【答案】AC
【解析】解:A.反应C﹣C变为C=C,为消去反应,故A正确;
B.乙苯的同分异构体可为二甲苯,有邻、间、对,连同乙苯共4种,如不含苯环,则同分异构体种类更多,故B错误;
C.苯乙烯可与溴发生加成反应,溶液褪色,而乙苯不反应,可鉴别,故C正确;
D.苯环和碳碳双键都为平面形,与苯环直接相连的原子在同一个平面上,则乙苯有7个碳原子共平面,苯乙烯有8个碳原子共平面,故D错误.
故选AC.
A.根据反应C﹣C变为C=C的特点判断; B.乙苯的同分异构体可为二甲苯,有邻、间、对等,也可能不含苯环; C.苯乙烯可与溴发生加成反应; D.苯环和碳碳双键都为平面形,与苯环直接相连的原子在同一个平面上.


科目:高中化学 来源: 题型:
【题目】一定量的浓硝酸与44.8g的铜反应,铜片完全溶解后收集到标况下混合气体NO和NO2的体积为22.4L,不考虑NO2与N2O4的相互转化,试计算下列相关问题:(要求写出计算过程)
(1)消耗的硝酸物质的量.
(2)混合气体中NO2、NO的体积.
(3)相同条件下,上述反应生成的NO2、NO分别被水恰好吸收时所需的O2体积比.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室产生的废液中含有Fe3+、Cu2+、Ag+三种金属离子,实验室设计了方案对废液进行以下三步处理,并回收金属.
请回答:
(1)步骤①中得到的沉淀含有的金属单质有 .
(2)步骤②是将Fe2+转化为Fe3+ , 还可以选用的试剂是 .
A.Fe粉
B.NaOH溶液
C.新制氯水
D.稀硫酸
(3)步骤③中加入氨水生成红褐色沉淀的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示的原电池,下列说法正确的是( ) 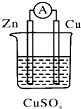
A.电流从锌电极通过电流表流向铜电极
B.锌电极发生还原反应,铜电极发生氧化反应
C.当有13 g Zn溶解时,外电路中就有0.4 mol电子通过
D.铜电极作正极,发生的电极反应为2H++2e﹣═H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,参照元素在表中的位置,请用化学用语回答下列问题:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
1 | ① | |||||||
2 | ⑤ | ⑥ | ⑦ | |||||
3 | ② | ③ | ④ | ⑧ | ||||
4 | ⑨ | |||||||
5 | ⑩ |
(1)元素⑥的名称为;⑨的最高价含氧酸的化学式为 .
(2)①和⑦两种元素的原子按1:1组成的常见化合物的结构式为 .
(3)③、④、⑦、⑧的简单离子半径由大到小的顺序为 . (用离子符号表示)
(4)②、④的最高价氧化物的水化物之间发生反应的离子方程式 .
(5)用电子式表示③和⑨组成的化合物的形成过程 .
(6)海带中含有⑩元素,海带灰中含有该元素的简单阴离子,在硫酸酸化下,可用双氧水将其氧化为单质.写出该反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能在溶液中大量共存的一组离子是( )
A.Cu2+、SO ![]() 、OH﹣、K+
、OH﹣、K+
B.Fe3+、SCN﹣、Cl﹣、H+
C.K+、CO ![]() 、Cl﹣、H+
、Cl﹣、H+
D.H+、Na+、Cl﹣、SO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)反应3A(g)+B(g)═2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1 mol/(Lmin)、②vC=0.5mol/(Lmin)、③vB=0.5mol/(Lmin),三种情况下该反应速率由大到小的关系是 . (用序号表示)
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的量随时间的变化曲线如图所示.根据图中数据填空: 
①该反应的化学方程式为 .
②反应开始至2min,以气体Z表示的平均反应速率为 .
③2min反应达平衡容器内混合气体的平均相对分子质量比起始时(填“大”,“小”或“相等”下同),混合气体密度比起始时 .
④上述反应,在第2min时,X的转化率为 .
⑤将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X)=n (Y)=n (Z),则原混合气体中a:b= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)实验室从含碘废液(除H2O 外,含有CCl4、I2、I﹣等)中回收碘,其实验过程中有一步向含碘废液中加入稍过量的Na2SO3 溶液,将废液中的I2 还原为I﹣ , 其离子方程式为;
(2)MnO2可与KOH和KClO3在高温条件下反应,生成K2MnO4 , 反应的化学方程式为 , K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为 .
(3)K2Cr2O7是一种橙红色具有强氧化性的化合物,在硫酸酸性条件下被还原成三价铬时,颜色变为绿色.据此,当交警发现汽车行驶不正常时,就可上前阻拦,并让司机对填充了吸附有K2Cr2O7的硅胶颗粒的装置吹气.若发现硅胶变色达到一定程度,即可证明司机是酒后驾车.这时酒精被氧化为醋酸,请写出该反应的化学方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com