
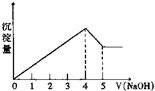
 有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量比为( )
有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量比为( )| A. | 2:1 | B. | 4:1 | C. | 1:2 | D. | 1:1 |
分析 氢氧化钠的体积为0~4时,发生的反应为:Al3++3OH-═Al(OH)3↓,Mg2++2OH-═Mg(OH)2↓,氢氧化钠的体积为4~5时发生的反应为:Al(OH)3+NaOH═NaAlO2+2H2O,假设氢氧化铝溶解消耗氢氧化钠为1mol,则沉淀最大时消耗NaOH为4mol,结合方程式计算n[Al(OH)3],进而计算n[Mg(OH)2],由原子守恒知n(Al)=n[Al(OH)3],n(Mg)=n[Mg(OH)2],据此进行计算.
解答 解:氢氧化钠的体积为0~4时,发生的反应有:Al3++3OH-═Al(OH)3↓,Mg2++2OH-═Mg(OH)2↓,氢氧化钠的体积为4~5时发生的反应为:Al(OH)3+NaOH═NaAlO2+2H2O,
假设氢氧化铝溶解消耗氢氧化钠为1mol,则沉淀最大时消耗NaOH为4mol,
由Al(OH)3+NaOH═NaAlO2+2H2O可知,n[Al(OH)3]=n(NaOH)=1mol,
Al3++3OH-═Al(OH)3↓
3mol 1mol
生成氢氧化镁沉淀消耗NaOH为4mol-3mol=1mol,由Mg2++2OH-═Mg(OH)2↓可知n[Mg(OH)2]=0.5mol,
由原子守恒知n(Al)=n[Al(OH)3]=1mol,n(Mg)=n[Mg(OH)2]=0.5mol,
故原合金中镁、铝物质的量之比为0.5mol:1mol=1:2,
故选C.
点评 本题考查镁铝单质及其化合物的性质、混合物的有关计算,明确各阶段发生的反应是解题的关键,注意利用赋值法计算,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO的结构式:H-O-Cl | B. | H2O2的电子式: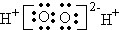 | ||
| C. | 质量数为14碳原子表示方法:14C | D. | 14C的原子结构示意图: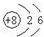 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积相等pH=12的氨水和NaOH溶液中和盐酸的能力相同 | |
| B. | 室温下,向NH4HSO4溶液中加入NaOH溶液至中性,则c(SO42-)>c(Na+)>c(NH4+) | |
| C. | 物质的量浓度之比为1:2的CH3COOH和CH3COONa的混合溶液中:2c(CH3COO-)+2c(CH3COOH)=3c(Na+) | |
| D. | 向10ml 0.01mol/L AgNO3溶液中依次滴入2~3滴0.01mol/L NaCl溶液、0.01mol/L NaI溶液,所得沉淀由白色变成黄色,则可推知Kap(AgI)<Kap(AgCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH的摩尔质量为40 g | |
| B. | 1 mol O2的质量与它的相对分子质量相等 | |
| C. | 1 mol OH-的质量为17 g•mol-1 | |
| D. | 氦气的摩尔质量(单位g•mol-1)在数值上等于它的相对原子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎把少量的浓硫酸沾在手上,应立即用大量水冲洗,然后涂上碳酸氢钠溶液 | |
| B. | 不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 如果汽油、煤油等可燃物着火,应立即用水扑灭 | |
| D. | 酒精灯不慎碰翻着火,应立即用湿布盖灭 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com