
����ѧ��ѡ��5���л���ѧ������
��Ⱦ�����Чȥ������Դ�ij�������ǻ�ѧ�츣�������Ҫ�о����⡣ij�о�С���������̿�(��Ҫ�ɷ�ΪMnO2��������������������ͭ�����Ƚ���������)���������ͨ�����¼����̼��ѳ�ȼúβ���е�SO2�����Ƶõ�ز���MnO2����Ӧ������ʡ�ԣ���
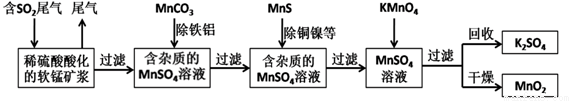
��ش��������⣺
(1)���������ж����Ƶ����˲�����ʵ���ҽ��й��˲���ʱ��Ҫ�õ��Ĺ����������в��������ձ���_______________�����в�������������___________________��
(2)��MnCO3�ܳ�ȥ��Һ�е�Al3+��Fe3+����ԭ����_____________(ֻ�����ֱ���)
(3)��ҵ�ϲ��õ��K2MnO4ˮ��Һ�ķ���������KMnO4�����ж��Ե缫��������������������д�������ĵ缫��Ӧʽ__________________��
(4)���и����Լ��У���ȷ�ⶨһ�����ȼúβ����SO2��������__________��(����)
a��NaOH��Һ����̪��Һ b��ϡH2SO4�ữ��KMnO4��Һ
c����ˮ��������Һ d����ˮ����̪��Һ
(5)������SO2��ϡ�����ữ�����̿�Ӧ�Ļ�ѧ����ʽΪ_______________����֪������SO2Ũ��Ϊ6.4g/m3�����̿�SO2�������ʿɴ�90%������1000m3ȼúβ�����ɵõ������̾���(MnSO4��H2O����Է�������Ϊ169)����Ϊ_________________kg(�������3 λ��Ч����)��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ʡ����ģ���Ļ�ѧ���������棩 ���ͣ�ѡ����
��(Ga)����ͬ���壬������Ϊ����������������������������Ϊ���Ի������ҵ�Ʊ��ص���������ͼ��ʾ��
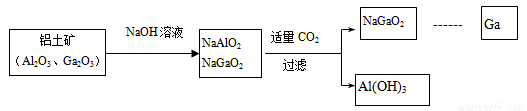
�����жϲ��������ǣ�
A. Al��Ga������IIIA��
B. Ga2O3�������ᷴӦ����GaCl3
C. Ga(OH)3����NaOH��Ӧ����NaGaO2
D. ���ԣ�Al(OH)3>Ga(OH)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ĸ������¿��廯ѧ�Ծ��������棩 ���ͣ������
����ʮ���صij���F�Ľ��ͻ���ƽ���֮һΪ��ɫ����N2O4��N2O4��NO2ת�����Ȼ�ѧ����ʽΪ��N2O4(g) 2NO2(g) ��H=+24.4KJ/mol
2NO2(g) ��H=+24.4KJ/mol
(1)��һ����N2O4Ͷ��̶��ݻ�����������У�����������˵����Ӧ�ﵽƽ����� ��
a�� v��(N2O4)=2v��(NO2) b����ϵ��ɫ����
v��(N2O4)=2v��(NO2) b����ϵ��ɫ����
c������ƽ����Է����������� d�������ܶȲ���
�ﵽƽ�����������������¶ȣ��ٴε���ƽ��ʱ������������ɫ (����������dz�����䡱)���ж����� ��
��2)T��ʱ����1L�����ܱ�������Ͷ��1molCH4��1molH2O(g)��������Ӧ��CH4(g)+H2O(g) CO(g)+3H2(g)������3min����Ӧ�ﵽƽ�⡣��֪ƽ��ʱc(CH4
CO(g)+3H2(g)������3min����Ӧ�ﵽƽ�⡣��֪ƽ��ʱc(CH4 )=0.5mol/L
)=0.5mol/L
��0��3min�ڣ��÷�Ӧ��ƽ����Ӧ����v(H2)=____________��
��T��ʱ���÷�Ӧ��ƽ�ⳣ��K=___________��
(3)��һ����������CO��H2�����Ƶü״���CH3OH��C O��ȼ����Ϊ��725.8 kJ/mol ��283.0 kJ/mol��1 molҺ̬ˮ�����̬ˮ����44.0 kJ��д���״�����ȫȼ������һ����̼����̬ˮ���Ȼ�ѧ����ʽ�� ��
O��ȼ����Ϊ��725.8 kJ/mol ��283.0 kJ/mol��1 molҺ̬ˮ�����̬ˮ����44.0 kJ��д���״�����ȫȼ������һ����̼����̬ˮ���Ȼ�ѧ����ʽ�� ��
(4)��ҵ����CO��H2�ڴ��������ºϳ�CH3OH,�䷴ӦΪ��CO(g)+2H2(g) CH3OH(g)����n(CO) : n(H2)=1 : 2���ܱ������г��뷴Ӧ����ƽ��ʱ�������CH3OH����������ڲ�ͬѹǿ�����¶ȵı仯��ͼ��ʾ��
CH3OH(g)����n(CO) : n(H2)=1 : 2���ܱ������г��뷴Ӧ����ƽ��ʱ�������CH3OH����������ڲ�ͬѹǿ�����¶ȵı仯��ͼ��ʾ��
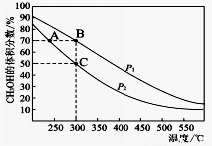
P1_________P2(�<����>����=��)
����C��ʱ��COת����Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ĸ������¿�����ѧ���������棩 ���ͣ�ѡ����
п-����ȼ�ϵ�ؿ������綯��������Դ����صĵ������ҺΪKOH��Һ����ӦΪ2Zn+O2+4OH�C+2H2O=2Zn(OH)42-������˵����ȷ����
A�����ʱ���������Һ��K+�������ƶ�
B�����ʱ���������Һ��c��OH-����С
C���ŵ�ʱ��������ӦΪ��Zn+4OH�C-2e�C=Zn(OH)42-
D���ŵ�ʱ����·��ͨ��2mol���ӣ���������22.4L����״����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ĸ������¿�����ѧ���������棩 ���ͣ�ѡ����
���и�����������ˮ��Һ�д����������
A��Ca2+��SO42-��H+��HCO3- B��H+��NO3-��Cl-��SiO32-
C��K+��Fe2+��H+��NO3- D��K+��Na+��CO32-��SiO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ĸ�������Ӧ��ѵ���Ļ�ѧ���������棩 ���ͣ�ѡ����
��ϵ����������ڹ�������±�ɫ�������������Լ���绯ѧ���������Ź㷺��Ӧ�ú����˵�ǰ����ʵ�����п�����FeCO3��O2Ϊԭ���Ʊ��������죬ÿ����160g��������ų�130kJ�������������йظ÷�Ӧ���Ȼ�ѧ����ʽ��д��ȷ����
A. 2FeCO3 +1/2O2 =Fe2O3 +2CO2 ��H��-130 kJ/mol
B. 4FeCO3(s)��O2 (g) =2Fe2O3(s)+4CO2(g) ��H��+260 kJ/mol
C. 4FeCO3(s)��O2 (g) =2Fe2O3(s)+4CO2(g) ��H��+130 kJ/mol
D. 4FeCO3(s)��O2 (g) =2Fe2O3(s)+4CO2(g) ��H��-260 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ�����϶ο�����ѧ�Ծ��������棩 ���ͣ�ʵ����
����������һ����Ҫ�Ļ�����Ʒ���ڹ�ҵ������Ҫ����;��ijУ��ѧ��ȤС�飬���ù�ҵ����Ϊԭ�ϣ���������Ʊ����������ķ�����ѧ��̽����������Ҫ�ɷ�Ϊ���������P����FeS��SiO2 �ȣ��Ʊ��̷���FeSO4��7H2O������������������ʾ��
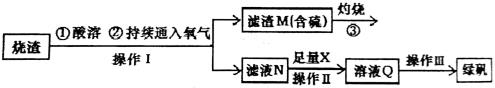
��1�������ڽ�������ʱ�õ���ϡ���ᡣ���������������ϡ����ʱʹ��������ˮ����ͬѧ�������ˮ�к���������Cl-����Ӱ�쵽�Ƴ���FeSO4 �Ĵ��ȡ��������ʵ��֤�������Ƶ�ϡ�����л���Cl-��
_______________________��
��2�����̢�����ʱ����������ͨ��������Һ�У� ��Һ������ɫ����___________
��Һ������ɫ����___________
A��Ʒ����Һ B����ɫʯ����Һ C������KMnO4��Һ D����ɫ�ķ�̪��Һ
��3��X �� �� ��ʱ��ҺN �з�����Ӧ�����ӷ���ʽΪ ��������ҺQ �к��еĽ��������ӵ�ʵ�鷽���� ��
��4������III �IJ�������Ϊ����Ũ���� �����ˣ� ��������ƣ���  �����
�����
��5����������������������ȱ����ƶѪ֢��ij����ƶѪ���߹��貹��2.8g��Ԫ�أ����õ�ҩƷ���൱����Ҫ�̷�������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪�ֳ��������ѧУ��һ����ĩ�Ļ�ѧ���������棩 ���ͣ�ѡ����
����(Fe2O3)��������ɫ�����Ϳ�ϡ������й�Fe2O3��������ȷ���� 
A���ܸ����ᷴӦ B��������ˮ C���ڿ������ױ����� D���д���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪�ֳ��������ѧУ��һ����ĩ����ѧ���������棩 ���ͣ�ѡ����
����˵����ȷ����( )
A��6.02��1023�����ӵ����Լ��22.4L
B��0.5mol H2�����Ϊ11.2L
C����״���£�1mol H2O�����Ϊ22.4L
D����״���£������ͬ�����������ķ�������ͬ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com