
����һ�ֿ����ھ�ˮ����ʳƷ���Σ���A��B��C��D��E���ֶ�����Ԫ����ɡ�������ˮ��ɵ�����������ӣ�����һ������A��B�γɵ�10���������ӡ�AԪ��ԭ�Ӻ�����������E����l��D��Eͬ���塣ijͬѧΪ̽������ɶ���������ʵ�飺
��ȡmg�ľ�����������ˮ�����500 mL��Һ��
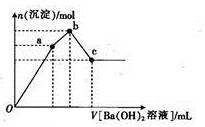
��ȡ��������Һ���Թ��У���ε���Ba(OH)2��Һ�����ɳ��������ʵ��������Ba(OH)2��Һ����Ĺ�ϵ��ͼ��ʾ��
��ȡ20 mL����Һ���Թ��У��������NaOH��Һ����Ȳ��ռ����������壬Ȼ������ɱ�״���µ����Ϊ224 mL��
�ش��������⣺
��1��D��Ԫ�����ڱ��е�λ��Ϊ_ ��
��2�����ⶨ�����Ħ������Ϊ453 g��mol-1�����������Ӻ����������ʵ���֮��Ϊ1:1�� ����Ļ�ѧʽΪ_ _��
��3��ͼ����V(Oa)��V(ab)��V(bc)= _ ��
��4��д��ab�η�����Ӧ�����ӷ���ʽ��_ ��
��5����ɵļ���Һ���ʵ���Ũ����_ ��
 �������ͬ������ϵ�д�
�������ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶���ѧ�����б���ѧ�Ծ��������棩 ���ͣ�ѡ����
����Һ���ܴ����������������
A��Na+��OHһ��HCO3- B��Ba2+��OHһ��C1��
C��H+��K+��CO32-�� D��NH4+��NO3����OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ������ѧ�ڵڶ���ģ����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��1200��ʱ����Ȼ���������лᷢ�����з�Ӧ
��H2S(g)+ 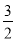 O2(g) = SO2(g)+H2O(g) ��H 1
O2(g) = SO2(g)+H2O(g) ��H 1
��2H2S(g)+SO2(g) =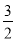 S2(g)+2H2O(g) ��H 2
S2(g)+2H2O(g) ��H 2
��H2S(g)+ O2(g) = S(g)+H2O(g) ��H 3
O2(g) = S(g)+H2O(g) ��H 3
��S(g) = 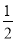 S2(g) ��H4
S2(g) ��H4
���H 4����ȷ����ʽΪ
A����H 4 =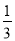 (3��H 3 - ��H 1 - ��H 2)
(3��H 3 - ��H 1 - ��H 2)
B�� ��H 4 = (��H 1 + ��H 2 - 3��H 3)
(��H 1 + ��H 2 - 3��H 3)
C����H 4 =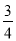 (��H 1 + ��H 2 - 3��H 3)
(��H 1 + ��H 2 - 3��H 3)
D����H 4 =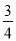 (��H 1 - ��H 2 - 3��H 3)
(��H 1 - ��H 2 - 3��H 3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʵ����ѧ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��ʹ������к͵ζ����ⶨ���۰״ף�CH3COOH����������(g/100 mL)��
��.ʵ�鲽�裺

��1����ȡ10.00 mLʳ�ð״ף����ձ�����ˮϡ�ͺ�ת�Ƶ�100 mL________(����������)�ж��ݣ�ҡ�ȼ��ô���״���Һ��
��2������ʽ�ζ���ȡ����״���Һ20.00 mL����ƿ�У������еμ�2��________��ָʾ����
��3����ȡʢװ0.100 0 mol/L NAOH��Һ�ļ�ʽ�ζ��ܵij�ʼ���������Һ��λ����ͼ��ʾ�����ʱ�Ķ���Ϊ________mL��
��4���ζ����ζ��յ��������__________________________________________��
��.���ݼ�¼��
����� | 1 | 2 | 3 | 4 |
V(��Ʒ) (mL) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NAOH)(����) (mL) | 15.95 | 15.00 | 15.05 | 14.95 |
��.���ݴ�����
ijͬѧ�ڴ�������ʱ����ã�
ƽ�����ĵ�NAOH��Һ�����V��(15.95��15.00��15.05��14.95)/4 mL��15.24 mL��
��5��ָ�����ļ���IJ�����֮����__________________������ȷ���ݴ������ɵ����۰״���������________g/100 mL��(���������λ��Ч����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫��ͷ��ɽ��ѧ��һ10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ͬ���ʵ���Ũ�ȵ�KCl��CaCl2��AlCl3������Һ�������Ϊ3:2:1����������Һ��Cl�����ʵ���Ũ��֮����
A��3:2:1 B��1:2:3 C��1:1:1 D��2:3:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016�ӱ�ʯ��ׯ��һ��ѧ��һ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�������
��1��8��4g N2��9��6gij����Rx����ԭ�Ӹ�����ͬ���ҷ�����֮��Ϊ3:2����R�����ԭ�������� ��xֵΪ ��
��2��4��5gˮ�� g���������ķ�������ȣ�����������ԭ����֮���� ��������ԭ����֮���� ��
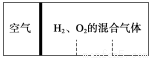
��3����ͼ��ʾ���ֱ����ܱ������ڿ��ƶ����������߳������(��֪�������ռ���������ݻ���1/4)��H2��O2�Ļ�����壬�ڱ�״���£�����H2��O2�Ļ�������ȼ���������������ָ�ԭ�¶Ⱥ����һ�ͣ�������������롣��ԭ��H2��O2�����֮�ȿ���Ϊ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016�ӱ�ʯ��ׯ��һ��ѧ�߶������п��Ի�ѧ�Ծ��������棩 ���ͣ������
ij��A����Է�������Ϊ84���ش��������⣺
��1������������A�����������ϣ��������ʵ���һ�������ȼ������������������ȵ���(�����) ��a��C7H12O2 b��C6H14 c��C6H14O d��C7H14O3
��2������AΪ��������HBr�ӳɺ�ֻ�ܵõ�һ�ֲ���Ҹ�����һ�ȴ���ֻ��һ�֡�
��A�Ľṹ��ʽΪ________________�������� ��
��A��һ���������ܷ����Ӿ۷�Ӧ��д���÷�Ӧ�Ļ�ѧ����ʽ ��
��A����������ˮ��Ӧ����B��B��NaOH�Ĵ���Һ���ȿ��Եõ�D��B��D����Է�����������M(D)+81=M(B)����D�����к��еĹ������� �������ƣ���
��3�����˴Ź���������ʾ����A���������壬�ҷ������Ϊ3��2��1��д��A���п��ܵĽṹ��
ʽ ������˳���칹����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ���� ( )
 A��̼�������Һ�м�������ʵ���������������Һ��
A��̼�������Һ�м�������ʵ���������������Һ�� Ca2++2HCO3-+2OH-=CaCO3��+2H2O+CO32-
Ca2++2HCO3-+2OH-=CaCO3��+2H2O+CO32-
B����NaAlO2��Һ�м���������Һ�����ԣ�A1O2-+4H+=Al3++2H2O
C����̼�������Һ�м��������NaOH��Һ��HCO3-+OH-=CO32-+H2 O
D��Cl2��H2O��Ӧ��Cl2+H2O=2H++Cl-+C1O-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016����ϳ�ɳ������ѧ�ڵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ������
��1�����ӹ�ҵ��ʹ�õ�һ����̼���Լ״�Ϊԭ��ͨ�����⡢�ֽ�������Ӧ�õ���
��һ����2CH3OH(g)  HCOOCH3(g)+2H2(g) ��H>O
HCOOCH3(g)+2H2(g) ��H>O
�ڶ�����HCOOCH3(g)  CH3OH(g)+CO(g) ��H>O
CH3OH(g)+CO(g) ��H>O
��һ����Ӧ�Ļ���������ͼ1��ʾ���м����X�Ľṹ��ʽΪ___________��
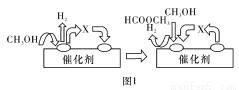

��2��Ϊ��������о�����CO��ԭ��������ʯ����Ӧ��������ʵ�X-����������ͼ��ͼ2��ʾ(X-��������������ж�ij��̬�����Ƿ���ڣ���ͬ��̬���ʳ�������������Dz�ͬ)����Ӧ�������е�һ�ֲ����������ᷴӦ���������Σ��÷�Ӧ�����ӷ���ʽΪ��_____________��
��3��ij������Ʒ(��Ni2O340%������ΪSiO2)ͨ����ԭ���ᴿ������������ʣ�������CO��33.2g��Ʒ�ڼ��������»�ԭΪ������Ȼ���ڳ�����ʹ�����е�Ni��CO��ϳ�Ni(CO)4��(�е�43��)������180��ʱʹNi(CO)4���·ֽ���������ʡ���������������CO�����ʵ���֮��Ϊ______________��
��4��Ϊ��ȫ�������ҵ��������Կ����е�CO���м�⡣ʹ�õ绯ѧһ����̼���崫����������������CO��������ṹ��ͼ3 ��ʾ�����ִ���������ԭ���ԭ������õ�صĸ�����ӦʽΪ��_____________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com