
| A.2.4 mL、O2 | B.1.2mL、NO | C.4 mL、O2 | D.3.6 mL、NO |
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.③④ | C.①③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.4:3:2 | B.9:3:16 | C.2:2:1 | D.9:3:8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.As2O3是砷的最高价含氧酸的酸酐        |
| B.As2O3的晶体为原子晶体 |
| C.如不慎As2O3不慎撒落河水中,可投入纯碱以消除污染 |
| D.如不慎As2O3不慎撒落河水中,可投入生石灰以消除污染 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
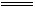 2CuO+4NO2+O2,某人将少量的Cu(NO3)2固体放入试管中加热,然后用带火星的木条放入试管中,木条复燃,则下列说法正确的是 ( )
2CuO+4NO2+O2,某人将少量的Cu(NO3)2固体放入试管中加热,然后用带火星的木条放入试管中,木条复燃,则下列说法正确的是 ( )| A.NO2能支持燃烧 | B.NO2不能支持燃烧 |
| C.木条复燃是因为硝酸铜分解产生了氧气的缘故 | |
| D.木条复燃是因为硝酸铜分解产生了氧气和二氧化氮共同作用的结果 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NO3- | B.NO2- | C.NH4+ | D.有机氮 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com