
用质量均为100g的铜作电极,电解硝酸银溶液(足量),电解一段时间后,两电极的质量差为28g,此时两电极的质量分别为( )
| A.阳极100g,阴极128g | B.阳极93.6g,阴极121.6g |
| C.阳极91.0g,阴极119.0g | D.阳极86.0g,阴极114.0g |
科目:高中化学 来源: 题型:单选题
把甲、乙、丙、丁四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若甲、乙相连,甲的质量减少;丙、丁相连,丁上有气泡逸出;甲、丙相连,甲上发生氧化反应;乙、丁相连,乙是电子流入的一极。则四种金属的活泼性顺序由大到小排列为
| A.甲>乙>丙>丁 | B.甲>丙>乙>丁 |
| C.甲>丙>丁>乙 | D.乙>丁>丙>甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图是电解CuCl2溶液的装置,其中c、d为石墨电极。下列说法不正确的是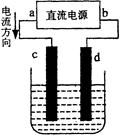
| A.a为正极、b为负极 |
| B.c为阳极、d为阴极 |
| C.电解过程中,d电极质量增加 |
| D.电解过程中,氯离子浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72+6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确是
| A.阳极反应为Fe-2e- =Fe2+ |
| B.电解过程中溶液pH不会变化 |
| C.过程中有Fe(OH)3沉淀生成 |
| D.电路中每转移12 mol电子,最多有1 mol Cr2O72-被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某研究性学习小组进行电化学实验,研究装置如图所示。
有关说法不正确的是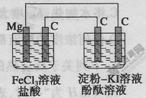
| A.镁为负极 |
| B.原电池中碳极的电极反应式为Fe3++e-=Fe2+ |
| C.电解池中阳极处先变红 |
| D.电解池中阴极的电极反应式为2H++2e-=H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
锂~碘电池可用来为心脏起搏器提供能源,其电池反应可表示为:2Li + I2 →2LiI。下列有关说法错误的是
| A.放电时化学能转化为电能 | B.负极反应为:Li –e→Li+ |
| C.正极反应为:I2+2e →2I- | D.电子由正极流向负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有A、B、C、D四块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极; ②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D 导线
导线 C ; ③ A、C用导线相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡; ④B、D用导线相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应。据此,判断四种金属的活动性顺序是
C ; ③ A、C用导线相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡; ④B、D用导线相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应。据此,判断四种金属的活动性顺序是
A. A>B>C>D B. A>C>D>B C. C>A>D>B D.C>B>D>A
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成下图所示的原电池。下列判断不正确的是

A.为证明反应的发生,可取甲中溶液加入酸性高锰酸钾溶液 |
B.反应开始时,甲中石墨电极上Fe3+被还原,乙中石墨电极上发生氧化反应 |
C.电流计读数为零时,在甲中加入FeCl2固体后,甲中石墨电极为负极 |
| D.此反应正反应方向若为放热反应,电流计读数为零时,降低温度后,乙中石墨电极为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用惰性电极电解一定量的硫酸铜溶液,实验装置如图1所示。电解过程中的实验数据如图2所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标况)。则下列说法中正确的是

| A.电解过程中,b电极表面先有红色物质析出,然后才有气泡产生 |
| B.从开始到Q点时收集到的混合气体的平均相对分子质量为17 |
| C.曲线OP 段表示H2和O2混合气体的体积变化,曲线PQ段表示O2的体积变化 |
| D.a电极上发生反应的方程式为:2H+ + 2e- = H2↑和4OH-–4 e-=2H2O+ O2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com