
����Ŀ����Ҫ������������
��1����0.6mol Al2��SO4��3�У�Al3+�ĸ���Ϊ �� �ڱ�״���µ�11.2L���������е�ԭ�ӵ���ĿΪ �� ij�����Ȼ���MCl281g������1.20molCl�� �� ����Ȼ����Ħ������Ϊ ��
��2��4mol��NH3��mol��H2S������ͬ����ԭ�ӣ���ͬ������C02��CO������ԭ�ӵ����ʵ���֮��Ϊ �� ������ԭ������ͬ��C02��CO�����ʵ���֮��Ϊ �� ��״���������Ϊ ��
��3�����У������ͺ��Ȼ�����Һ ��39%�ľƾ���Һ���������ϻ��Һ����ȷ������������������ˡ�������Һ�������ᾧ����������
���𰸡�
��1��1.2NA,NA,135g��mol��1
��2��6,14��11,1��2,1��2
��3����Һ,����
���������⣺��1����0.6mol Al2��SO4��3�У�Al3+Ϊ1.2mol��Al3+�ĸ���Ϊ1.2NA����״���µ�11.2L������n= ![]() =0.5mol�����е�ԭ�ӵ���ĿΪ0.5mol��2��NA=NA��ij�����Ȼ���MCl281g������1.20molCl������n��MCl2��=0.6mol��M=
=0.5mol�����е�ԭ�ӵ���ĿΪ0.5mol��2��NA=NA��ij�����Ȼ���MCl281g������1.20molCl������n��MCl2��=0.6mol��M= ![]() =
= ![]() =135g��mol��1��
=135g��mol��1��
���Դ��ǣ�1.2NA��NA��135g��mol��1��
��2��������ͬ����ԭ�ӣ���H�����ʵ�����Ϊ4mol��3=12mol��H2S�����ʵ���Ϊ ![]() =6mol����ͬ������C02��CO������ԭ�ӵ����ʵ����ֱ�Ϊ
=6mol����ͬ������C02��CO������ԭ�ӵ����ʵ����ֱ�Ϊ ![]() ��
�� ![]() �����ʵ�����Ϊ
�����ʵ�����Ϊ ![]() ��
�� ![]() =14��11����ԭ������ͬ��C02��CO����Oԭ�Ӿ�Ϊ2mol���������ʵ����ֱ�Ϊ1mol��2mol��������ԭ������ͬ��C02��CO�����ʵ���֮��Ϊ1��2����V=nVm��֪����״���������Ϊ1��2��
=14��11����ԭ������ͬ��C02��CO����Oԭ�Ӿ�Ϊ2mol���������ʵ����ֱ�Ϊ1mol��2mol��������ԭ������ͬ��C02��CO�����ʵ���֮��Ϊ1��2����V=nVm��֪����״���������Ϊ1��2��
���Դ��ǣ�6��14��11��1��2��1��2��
��3�������ͺ��Ȼ�����Һ�Ļ����ֲ㣬��ѡ���Һ�����룻 ��39%�ľƾ���Һ�оƾ���ˮ���ܣ����е㲻ͬ����ѡ�������룬
���Դ��ǣ���Һ������


 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ijBa��OH��2��Һ����μ���pH=x�����ᣬ��û����Һ�IJ���pH�����ʾ��
��� | ����������Һ�����/mL | ��������/mL | ��Һ��pH |
�� | 22.00 | 0.00 | 13 |
�� | 22.00 | 18.00 | 12 |
�� | 22.00 | 22.00 | 7 |
��1��Ba��OH��2��Һ�����ʵ���Ũ��Ϊ��
��2��x��ֵ�Ƕ��٣�
��3����100mL����Ba��OH��2��Һ����μ���0.05mol/L NaHCO3��Һ���������պô����ֵʱ��Һ��pHΪ���٣�����֪lg2=0.3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�ͨ�����з�Ӧ��ʵ��ȼú��������Ļ��գ�
SO2��g��+2CO��g�� ![]() 2CO2��g��+S��s��
2CO2��g��+S��s��
����Ӧ�ں��ݵ��ܱ������н��У������й�˵����ȷ���ǣ� ��
A.ƽ��ǰ�����ŷ�Ӧ�Ľ��У�������ѹǿʼ�ղ���
B.ƽ��ʱ�������������䣬�����������Ӧ���ʼӿ�
C.ƽ��ʱ���������¶ȣ�CO�������������÷�Ӧ�ġ�H��0
D.�����������䣬ʹ�ò�ͬ�������÷�Ӧƽ�ⳣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ���Ļ�ѧ֪ʶ���������з�Ӧ�Ļ�ѧ����ʽ������ǣ�������
A.2KNO3+S+3C�TK2S+N2��+3CO2��
B.2KMnO4+3H2O2+3H2SO4�T2K2SO4+2MnSO4+4O2��+6H2O
C.5KI+KIO3+6HCl�T6KCl+3I2+3H2O
D.4HCl��Ũ��+MnO2 ![]() MnCl2+2H2O+Cl2��
MnCl2+2H2O+Cl2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ı�0.1 ![]() ��Ԫ����
��Ԫ���� ![]() ��Һ��pH����Һ�е�
��Һ��pH����Һ�е� ![]() ��
�� ![]()
![]() �����ʵ�������
�����ʵ������� ![]() ��pH�ı仯��ͼ��ʾ[��֪
��pH�ı仯��ͼ��ʾ[��֪ ![]() ]��
]�� 
��������������ǣ� ��
A.pH=1.2ʱ�� ![]()
B.![]()
C.Ph=2.7ʱ�� ![]()
D.pH=4.2ʱ�� ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѡ��������Ԫ��R��T��Q��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������Q���ʿ��Ƴɰ뵼����ϣ������ж���ȷ���ǣ� �� 
A.W�γɵ����Ӱ뾶����T�γɵ����Ӱ뾶
B.W�ĵ����ڹ���������ȼ������WO3
C.����������ˮ��������ԣ�R��Q
D.T�ǵؿ��к������Ľ���Ԫ�أ��䵥�ʵĻ�ѧ���ʽϻ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������и������ʷֱ�����������ˮ��ϲ������ú���Һ�����㣬��ˮ�㼸������ɫ����( )
A. ʳ��ˮB. ��ϩC. ����D. �Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��3�����ʽṹ������]��15�֣�
�ҹ���ѧ������ɹ��ϳ������������嵪��������(N5)6(H3O)3(NH4)4Cl����R���������ش��������⣺
��1����ԭ�Ӽ۲���ӶԵĹ������ʽ�������Ų�ͼ��Ϊ��
��2��Ԫ�صĻ�̬��̬ԭ�ӵõ�һ�������γ���̬��һ������ʱ���ų�������������һ�������ܣ�E1�����ڶ����ڲ���Ԫ�ص�E1�仯������ͼ��a����ʾ�����г���Ԫ���⣬����Ԫ�ص�E1����������������ԭ��������Ԫ�ص�E1�����쳣��ԭ������
��3����X���������û�����R�ľ���ṹ����ֲ��ṹ��ͼ��b����ʾ��
�ٴӽṹ�Ƕȷ�����R�����������ӵ���֮ͬ��Ϊ �� ��֮ͬ��Ϊ�������ţ�
A.����ԭ�ӵ��ӻ�������� B.����ԭ�ӵļ۲���Ӷ���
C.����ṹ D.���ۼ�����
��R��������N5-�еĦҼ�����Ϊ���������еĴ�м����÷��� ![]() ��ʾ������m���������γɵĴ�м�ԭ������n���������γɵĴ�м����������籽�����еĴ�м��ɱ�ʾΪ
��ʾ������m���������γɵĴ�м�ԭ������n���������γɵĴ�м����������籽�����еĴ�м��ɱ�ʾΪ ![]() ������N5-�еĴ�м�Ӧ��ʾΪ��
������N5-�еĴ�м�Ӧ��ʾΪ��
��ͼ��b�������ߴ�����������ʾʽΪ��NH4+��N-H��Cl������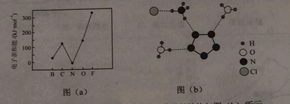
��4��R�ľ����ܶ�Ϊdg��cm-3 �� ��������������Ϊanm�������к���y��[(N5)6(H3O)3(NH4)4Cl]��Ԫ���õ�Ԫ���������ΪM �� ��y�ļ������ʽΪ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ֪ʶ�������Ŀ��
��1����25�������½�pH=11�İ�ˮϡ��100������Һ��pHΪ������ţ� ��
A.9
B.13
C.11��13֮��
D.9��11֮��
��2��25��ʱ����0.1molL��1�İ�ˮ�м�����������粒��壬�������ܽ�����ҺpH��С����Ҫԭ���ǣ�����ţ� ��
A.��ˮ���Ȼ�立�����ѧ��Ӧ
B.�Ȼ����Һˮ�������ԣ�������c��H+��
C.�Ȼ������ˮ����������������ӣ������˰�ˮ�ĵ��룬ʹc��OH����С
��3�������£������0.1mol NH4Cl��0.05molNaOHȫ������ˮ���γɻ����Һ����������ʧ�������������ӵ����ʵ���֮�͵���0.1mol��
�����������ӵ����ʵ���֮�ͱ�OH����0.05mol��
��4����֪ij��Һ��ֻ����OH����H+��NH4+��Cl�������ӣ�ijͬѧ�Ʋ����Һ�и�����Ũ�ȴ�С˳��������������ֹ�ϵ��A��c��Cl������c��NH ![]() ����c��H+����c��OH����B��c��Cl������c��NH
����c��H+����c��OH����B��c��Cl������c��NH ![]() ����c��OH+����c��H+��
����c��OH+����c��H+��
C��c��Cl������c��H+����c��NH ![]() ����c��OH����D��c��NH
����c��OH����D��c��NH ![]() ����c��Cl������c��OH������c��H+��
����c��Cl������c��OH������c��H+��
������Һ��ֻ�ܽ���һ�����ʣ��������� �� ��������Ũ�ȴ�С˳���ϵ����ȷ���ǣ�ѡ����ţ� ��
����������ϵ��C����ȷ�ģ�����Һ�����ʵĻ�ѧʽ�� ��
��������Һ���������ȵ�ϡ����Ͱ�ˮ��϶��ɣ���ǡ�ó����ԣ�����ǰc��HCl�������������������=������ͬ��c��NH3H2O������Ϻ���Һ��c��NH ![]() ����c��Cl�����Ĺ�ϵ��c��NH
����c��Cl�����Ĺ�ϵ��c��NH ![]() ��c��Cl������
��c��Cl������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com