
| A.1:1 | B.2:1 | C.3:1 | D.4:1 |
科目:高中化学 来源:不详 题型:单选题
| A.CuSO4 |
| B.CuSO4·5H2O |
| C.CuO |
| D.Cu(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解池是将化学能转化为电能的装置 |
| B.电解池的阳极发生氧化反应,阴极发生还原反应 |
| C.电解熔融的氯化钠中阴极只能用铁不可用其它电极 |
| D.只可电解熔融的电解质,不能电解电解质溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
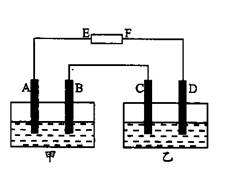
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
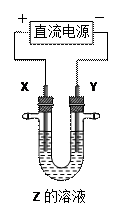
 产。下列说法中正确的是
产。下列说法中正确的是
A.氯碱工业中,X、Y均为石墨,Y附近能得到氢氧化钠 | B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4  | C.电镀工业中,X是待镀金属,Y是镀层金属 | D.外加电流的阴极保护法中,Y是待保护金属 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
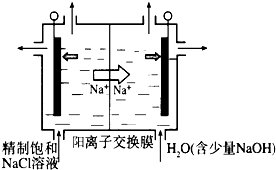
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
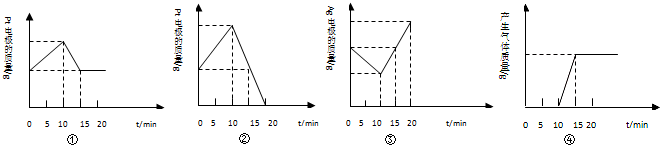
| A.①③ | B.①②③ | C.②③④ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com